摘要:在密闭容器内.使1mo1N2和3mo1H2混合发生下列反应:3H2+N2⇌2NH3. (1)当反应达到平衡时.N2和H2的浓度之比是 . (2)当升高平衡体系的温度.则混合气体的平均式量 .密度 . (3)当达到平衡时.充人N2并维持压强不变.平衡向 移动. (4)当达到平衡时.将[N2].[H2].[NH3]同时增大1倍.平衡向 移动. (5)当达到平衡时.充入Ar气.并保持体积不变.平衡 移动. (6)当达到平衡时.充入Ar气.并保持压强不变.平衡向 移动. 答案:减小,不变 正方向 逆方向 8.下面是合成NH3的简要流程示意图 (1)写出所含物质的化学式A .B .C . (2)写出设备的名称D .E . 答案:(1)A:N2和H2 B:NH3 C:N2H2 (2)D:合成塔 E:氨分离器 综合练习
网址:http://m.1010jiajiao.com/timu3_id_326257[举报]
在密闭容器内,使1mol N2 3mol H2混合发生下列反应:3H2+N2?2NH3 △H<0
(1)当反应达到平衡时,N2和H2的浓度比是
(2)保持体积不变,升高温度时,混合气体的平均相对分子是质量
(3)当达到平衡时,充入Ar气,并保持体积不变,平衡将
(4)当达到平衡时,充入Ar气,并保持压强不变,平衡将
(5)当达到平衡时,充入NH3气,并保持压强不变,平衡将
(6)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡将
查看习题详情和答案>>
(1)当反应达到平衡时,N2和H2的浓度比是
1:3
1:3
.(2)保持体积不变,升高温度时,混合气体的平均相对分子是质量
减少
减少
,密度不变
不变
.(填增大、减少或不变,第3~6题填“正向”、“逆向”或“不”)(3)当达到平衡时,充入Ar气,并保持体积不变,平衡将
不
不
移动.(4)当达到平衡时,充入Ar气,并保持压强不变,平衡将
逆向
逆向
移动.(5)当达到平衡时,充入NH3气,并保持压强不变,平衡将
逆向
逆向
移动.(6)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡将
正向
正向
移动.在密闭容器内,使1molN2和3molH2混合发生下列反应:N2+3H2?2NH3△H<0 (填“正向”、“逆向”或“不”)
(1)当达到平衡时,充入Ar气,并保持体积不变,平衡将
(2)当达到平衡时,充入Ar气,并保持压强不变,平衡将
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡将
查看习题详情和答案>>
(1)当达到平衡时,充入Ar气,并保持体积不变,平衡将
不
不
移动.(2)当达到平衡时,充入Ar气,并保持压强不变,平衡将
逆向
逆向
移动.(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡将
正向
正向
移动.(2013?南通一模)还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.
(1)利用炭粉可以将氮氧化物还原.
已知:N2(g)+O2(g)═2NO(g)△H=+180.6kJ?mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
反应:C(s)+2NO(g)═CO2(g)+N2(g)△H=
(2)TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,OH能将NO、NO2氧化,如图甲所示,OH与NO2的反应为NO2+OH═HNO3.写出OH与NO反应的化学方程式:
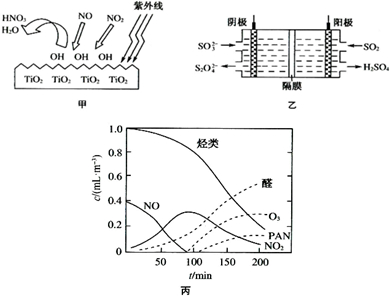
(3)图乙所示的装置能吸收和转化NO2、NO和SO2.
①阳极区的电极反应式为
②阴极排出的溶液中含S2
,离子能吸收NOx气体,生成的S
可在阴极区再生.将S2
吸收NO2的离子方程式配平,并在方格内填上相应物质:
+
+
③已知阴极生成的吸收液每吸收标准状况下7.84L的气体,阳极区新生成质量分数为49%的硫酸100g,则被吸收气体中NO2和NO的物质的量之比为
(4)O3、醛类、PAN(过氧硝酸乙酰)等污染物气体和颗粒物所形成的烟雾称为光化学烟雾.某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图丙所示.请你根据光化学烟雾的形成原理,对减少光化学烟雾的发生提出一个合理建议:
查看习题详情和答案>>
(1)利用炭粉可以将氮氧化物还原.
已知:N2(g)+O2(g)═2NO(g)△H=+180.6kJ?mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
反应:C(s)+2NO(g)═CO2(g)+N2(g)△H=
-574.1
-574.1
kJ?mol-1.(2)TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,OH能将NO、NO2氧化,如图甲所示,OH与NO2的反应为NO2+OH═HNO3.写出OH与NO反应的化学方程式:
3OH+NO═HNO3+H2O
3OH+NO═HNO3+H2O
.
(3)图乙所示的装置能吸收和转化NO2、NO和SO2.
①阳极区的电极反应式为
SO2-2e-+2H2O═SO42-+4H+
SO2-2e-+2H2O═SO42-+4H+
.②阴极排出的溶液中含S2
| O | 2- 4 |
| O | 2- 3 |
| O | 2- 4 |
4
4
S2| O | 2- 4 |
2
2
NO2+8
8
OH-═8
8
S| O | 2- 3 |
1
1
N2+4H2O
4H2O
③已知阴极生成的吸收液每吸收标准状况下7.84L的气体,阳极区新生成质量分数为49%的硫酸100g,则被吸收气体中NO2和NO的物质的量之比为
3:4
3:4
.(4)O3、醛类、PAN(过氧硝酸乙酰)等污染物气体和颗粒物所形成的烟雾称为光化学烟雾.某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图丙所示.请你根据光化学烟雾的形成原理,对减少光化学烟雾的发生提出一个合理建议:
减少机动车有害气体尾气的排放
减少机动车有害气体尾气的排放
.