摘要: 铁和硫酸铜溶液反应:Fe+CuSO4 = FeSO4+Cu
网址:http://m.1010jiajiao.com/timu3_id_31757[举报]
20、向硫酸铜和铁的混合物中,加入一定质量的稀硫酸当反应停止后,滤出不溶物,向滤液中放入一枚铁钉,发现铁钉并无任何变化,根据上述现象判断:滤出的不溶物中一定含有
查看习题详情和答案>>
Cu
:写出生成固体的化学变化的化学方程是Fe+CuSO4=Cu+FeSO4
.(2008?广安)向硫酸铜溶液中加入一定量的铁粉充分反应后,将所得固体过滤、洗涤.
(1)写出反应的化学方程式
(2)对所得固体的成分,提出三种猜想:①只有Fe,②只有Cu,③Fe和Cu的混合物.取少量上述固体,加入足量稀硫酸有气泡产生,说明猜想
(3)探究Zn、Cu的金属活动性强弱,下列试剂不能达到目的的是(填序号)
A.稀盐酸 B.硫酸镁溶液 C.氯化铜溶液.
查看习题详情和答案>>
(1)写出反应的化学方程式
Fe+CuSO4=Cu+FeSO4
Fe+CuSO4=Cu+FeSO4
.(2)对所得固体的成分,提出三种猜想:①只有Fe,②只有Cu,③Fe和Cu的混合物.取少量上述固体,加入足量稀硫酸有气泡产生,说明猜想
③
③
(填序号)正确.(3)探究Zn、Cu的金属活动性强弱,下列试剂不能达到目的的是(填序号)
B
B
.A.稀盐酸 B.硫酸镁溶液 C.氯化铜溶液.
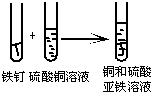 如图:反应前将铁钉和硫酸铜溶液放在天平上称量后取下,将铁钉放入硫酸铜溶液中发生反应的现象是铁钉表面有一层
如图:反应前将铁钉和硫酸铜溶液放在天平上称量后取下,将铁钉放入硫酸铜溶液中发生反应的现象是铁钉表面有一层红色
红色
固体生成,溶液由蓝色
蓝色
变为浅绿色
浅绿色
.发生反应的化学方程式是Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
.待反应完全后再将铜和硫酸亚铁溶液放在天平上称量,反应前后质量是否一样?一样
一样
.得到的结论是参加化学反应的各物质的质量总和,等于
等于
反应后生成的各物质的质量总和,用原子观点解释原因化学反应的过程,就是参加反应的各物质的原子,重新组合而生成其他物质的过程.在这个化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
化学反应的过程,就是参加反应的各物质的原子,重新组合而生成其他物质的过程.在这个化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
.(2012?泉州模拟)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程.
(1)黑色固体B的化学名为
(2)操作a的名称是
(3)反应①所发生化学反应的化学方程式为
(4)已知:Cu+2H2SO4 (浓)═CuSO4+SO2↑+2H2O.从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生
查看习题详情和答案>>

(1)黑色固体B的化学名为
氧化铜
氧化铜
;滤液1中的溶质为FeSO4(合理均可,与(3)对应)
FeSO4(合理均可,与(3)对应)
.(2)操作a的名称是
过滤
过滤
;操作a中需要的玻璃仪器有:漏斗
漏斗
、烧杯
烧杯
、玻璃棒
玻璃棒
.(3)反应①所发生化学反应的化学方程式为
Fe+H2SO4=FeSO4+H2↑(合理均可)
Fe+H2SO4=FeSO4+H2↑(合理均可)
;其反应为置换
置换
(选填“化合”、“分解”、“置换”或“复分解”)反应.(4)已知:Cu+2H2SO4 (浓)═CuSO4+SO2↑+2H2O.从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生
有害气体
有害气体
和硫酸的利用率高.