摘要:19.在100℃.将2.00mol的N2O4气体充人4L抽空的密闭容器中.隔一定时间对该容器内的物质进行分析.得到如下表格: 时 间/s 0 20 40 60 80 n(N2O4)/ mol 2.00 c1 1.00 c3 a n(NO2)/ mol 0 1.20 c2 2.4 2.4 (1)在0s-20s内N2O4的平均反应速率为 . (2)表中c2 c3 a(选填“> .“<’’或“= ).该反应的平衡常数为 . (3)若在相同情况下最初向该容器充人的是NO2气体.要达到上述同样的平衡状态. NO2的起始物质的量是 mol.
网址:http://m.1010jiajiao.com/timu3_id_313242[举报]
(2012?广东)苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
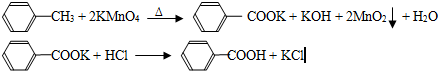
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为
(2)无色液体A是
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算表达式为
×100%;
×100%;,计算结果为
查看习题详情和答案>>

实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为
分液
分液
,操作Ⅱ为蒸馏
蒸馏
.(2)无色液体A是
甲苯
甲苯
,定性检验A的试剂是酸性KMnO4溶液
酸性KMnO4溶液
,现象是紫色溶液褪色
紫色溶液褪色
删去此空
删去此空
.(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解, 冷却 冷却 过滤 过滤 |
得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中, 滴入适量的硝酸酸化的AgNO3溶液 滴入适量的硝酸酸化的AgNO3溶液 |
生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, 加热使其融化,测其熔点 加热使其融化,测其熔点 |
熔点为122.4℃ 熔点为122.4℃ |
白色晶体是苯甲酸 |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
96%
96%
(保留二位有效数字).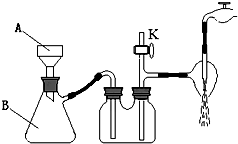 高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.
高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.(1)写出实验室制取高氯酸钾的化学方程式:
(2)用蒸馏水多次洗涤晶体的目的是
(3)称取29.8gKCl和34.0gNaNO3放入250mL烧杯中,再加入70.0g蒸馏水,制备KNO3晶体,I,使固体全部溶解.II,在100°C时蒸发掉50.0g水,维持该温度,趁热过滤析出晶体m1g.III,冷却结晶:待滤液冷却至室温(实验时室温为10°C)后,进行减压过滤.得KNO3粗产品m2g.IV,重结晶得KNO3纯品m3g.
查阅资料:文献中查得,四种盐在不同温度下的溶解度(S/g)如下表:
| NaNO3 | KNO3 | NaCl | KCl | |
| 10°C | 80.5 | 20.9 | 35.7 | 31.0 |
| 100°C | 175 | 246 | 39.1 | 56.6 |
②该装置有三处错误,分别是
③若实验过程中发现倒吸现象,应采取的措施是
(4)KNO3晶体纯品的产率
下面是四种盐在不同温度下的溶解度(克/100克水)
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计.)
(1)取23.4克NaCl和40.4克KNO3,加70.0克H2O,加热溶解.在100℃时蒸发掉50.0克H2O,维持该温度,过滤出晶体,计算所得晶体的质量(m高温).将滤液冷却至10℃,待充分结晶后,过滤.计算所得晶体的质量(m低温).
(2)另取34.0克NaNO3和29.8克KCl,同样进行如上实验.10℃时析出的晶体是
查看习题详情和答案>>
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
(1)取23.4克NaCl和40.4克KNO3,加70.0克H2O,加热溶解.在100℃时蒸发掉50.0克H2O,维持该温度,过滤出晶体,计算所得晶体的质量(m高温).将滤液冷却至10℃,待充分结晶后,过滤.计算所得晶体的质量(m低温).
(2)另取34.0克NaNO3和29.8克KCl,同样进行如上实验.10℃时析出的晶体是
KNO3和NaCl
KNO3和NaCl
(写化学式).100℃和10℃得到的晶体质量(m′高温和m′低温)分别是多少?已知100℃时水的离子积Kw是1.0×10-12,回答下列问题:
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为
(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为
查看习题详情和答案>>
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
1:9
1:9
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
5
5
.②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为
6
6
.(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
1:10:1010:109
1:10:1010:109
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为
11
11
.(2013?上海二模)碳酸钠俗称纯碱,其用途很广.实验室中,用碳酸氢铵和饱和食盐水可制得纯碱.各物质在不同温度下的溶解度见表.
实验步骤
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7.
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱.
(1)“化盐与精制”可除去的粗盐中的杂质离子是
(2)“转化”的离子方程式是
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是
(4)a,b处的操作分别是
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1 mL.此时发生的反应为:CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是
×100%
×100%.
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL.滴定终点时溶液颜色的变化是
查看习题详情和答案>>
| 温度℃ 溶解度 溶质 g/100g水 |
10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ||||
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7.
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,
a
a
、b
b
;③得到NaHCO3晶体.Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱.
(1)“化盐与精制”可除去的粗盐中的杂质离子是
Ca2+、Mg2+
Ca2+、Mg2+
.(2)“转化”的离子方程式是
Na++HCO3-=NaHCO3↓
Na++HCO3-=NaHCO3↓
.(3)“转化”过程中,温度控制在30~35℃之间的加热方式是
水浴加热
水浴加热
;为什么温度控制在30~35℃之间?温度过高造成NH4HCO3分解,温度过低NH4HCO3的溶解度小
温度过高造成NH4HCO3分解,温度过低NH4HCO3的溶解度小
.(4)a,b处的操作分别是
过滤
过滤
、洗涤
洗涤
.(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1 mL.此时发生的反应为:CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL.滴定终点时溶液颜色的变化是
黄色变为橙色且半分钟不变
黄色变为橙色且半分钟不变
;根据实验数据,如何判断样品含有NaHCO3V2>V1则含有NaHCO3
V2>V1则含有NaHCO3
.