摘要:27.硫酸钠是制造纸浆.染料稀释剂.医药品等的重要原料.某硫酸钠粗品中含有少量的氯化钙.氯化镁.实验室进行提纯的流程如下: (1)滤渣中两种主要成分的化学式为 ▲ . ▲ . (2)NaOH和Na2CO3如果添加过量了.可加入适量 ▲ 溶液除去. (3)“后续处理 的主要操作是蒸发.为了获得纯净的硫酸钠.应蒸发至 ▲ . A.完全蒸干时停止加热 B.快干时停止加热.利用余热蒸干 C.有大量固体析出时停止加热.过滤弃去剩余的少量溶液 (4)已知硫酸钠的溶解度随温度变化的曲线如右图所示.40℃时.硫酸钠的饱和溶液中溶质质量分数为 ▲ .将该饱和溶液升高温度至90℃.观察到的现象是 ▲ .
网址:http://m.1010jiajiao.com/timu3_id_30462[举报]
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和MgCl2,实验室进行提纯的流程如下: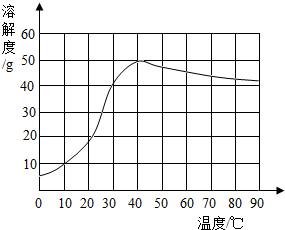
回答下列问题:
(1)操作A的名称是 ,该操作中需要用到的玻璃仪器有烧杯、 、 .
(2)加入氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为 、
.添加氢氧化钠和碳酸钠过量,可加入适量 溶液除去.(3)操作B是蒸发,为了得到较纯净的硫酸钠,应蒸发至 时,停止加热,利用余热蒸干.
(4)已知硫酸钠溶解度随温度变化的曲线如右图所示.40℃时,50g蒸馏水中溶解 硫酸钠达到饱和.将该饱和溶液升高温度到90℃,观察到的现象是 .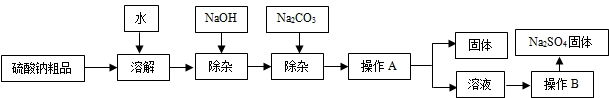 查看习题详情和答案>>
查看习题详情和答案>>

回答下列问题:
(1)操作A的名称是
(2)加入氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为
(4)已知硫酸钠溶解度随温度变化的曲线如右图所示.40℃时,50g蒸馏水中溶解
 查看习题详情和答案>>
查看习题详情和答案>>
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量的氯化钙、氯化镁,实验室进行提纯的流程如下:
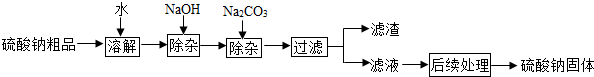
(1)滤渣中两种主要成分的化学式为 、 .
(2)NaOH和Na2CO3如果添加过量了,可加入适量 溶液除去.
(3)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至 (选填字母).
 A.完全蒸干时停止加热
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如图所示.40℃时,硫酸钠的饱和溶液中溶质质量分数为 (结果精确到0.1%),将该饱和溶液升高温度至90℃,观察到的现象是 .
查看习题详情和答案>>

(1)滤渣中两种主要成分的化学式为
(2)NaOH和Na2CO3如果添加过量了,可加入适量
(3)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至
 A.完全蒸干时停止加热
A.完全蒸干时停止加热B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如图所示.40℃时,硫酸钠的饱和溶液中溶质质量分数为
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaSO4和MgSO4,实验室进行提纯的流程如下(每一种试剂只除去一种杂质):
回答下列问题:
(1)试剂X是
(2)试剂X和试剂Y应该
查看习题详情和答案>>
回答下列问题:
(1)试剂X是
氢氧化钠溶液
氢氧化钠溶液
,试剂Y是碳酸钠溶液
碳酸钠溶液
;用X和Y除杂时,反应的化学方程式分别为2NaOH+MgSO4═Mg(OH)2↓+Na2SO4
2NaOH+MgSO4═Mg(OH)2↓+Na2SO4
、Na2CO3+CaSO4═CaCO3↓+Na2SO4
Na2CO3+CaSO4═CaCO3↓+Na2SO4
.(2)试剂X和试剂Y应该
过量
过量
(填“适量”或“过量”),理由是使硫酸钠粗品中的CaSO4和MgSO4全部反应
使硫酸钠粗品中的CaSO4和MgSO4全部反应
.
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaSO4和MgSO4,实验室进行提纯的流程如下:(提示:本题中微溶物质当可溶物质)
试回答下列问题:
(1)加入NaOH和Na2CO3时,反应的化学方程式分别为
(2)如果NaOH和Na2CO3添加过量了,可在过滤
(3)“后续处理”的主要操作是蒸发;蒸发时用玻璃棒不断搅拌,其作用是
查看习题详情和答案>>

试回答下列问题:
(1)加入NaOH和Na2CO3时,反应的化学方程式分别为
2NaOH+MgCl2═Mg(OH)2↓+2NaCl
2NaOH+MgCl2═Mg(OH)2↓+2NaCl
,Na2CO3+CaCl2═CaCO3↓+2NaCl
Na2CO3+CaCl2═CaCO3↓+2NaCl
.(2)如果NaOH和Na2CO3添加过量了,可在过滤
后
后
(填前或后)加入适量H2SO4
H2SO4
溶液.(3)“后续处理”的主要操作是蒸发;蒸发时用玻璃棒不断搅拌,其作用是
使液体均匀受热
使液体均匀受热
,蒸发操作中应有大量固体析出
有大量固体析出
时停止加热.硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和MgCl2,实验室进行提纯的流程如下:

(1)操作a的名称是
(2)写出沉淀b的成分
(3)NaOH和Na2C03如果添加过量了,可加入适量的
(4)若要用提纯后的硫酸钠固体来配制100g质量分数为10%的硫酸钠溶液,除了用到天平、药匙、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是
查看习题详情和答案>>

(1)操作a的名称是
过滤
过滤
,在实验室中进行此项操作时,若得到的溶液c仍然呈浑浊,其原因可能是滤纸破损
滤纸破损
.(写一条)(2)写出沉淀b的成分
Mg(OH)2、CaC03
Mg(OH)2、CaC03
(填化学式).(3)NaOH和Na2C03如果添加过量了,可加入适量的
H2SO4
H2SO4
(填化学式)溶液将其全部除去.(4)若要用提纯后的硫酸钠固体来配制100g质量分数为10%的硫酸钠溶液,除了用到天平、药匙、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是
玻璃棒
玻璃棒
,其作用是搅拌,加速溶解
搅拌,加速溶解
.