网址:http://m.1010jiajiao.com/timu3_id_298934[举报]
 ⅠA、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:
ⅠA、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:(1)各元素的符号:
A:
(2)写出C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序:
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:
ⅡFe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液),
(1)该反应的平衡常数K的表达式为:K=
| c2(Fe2+)×c(I2) |
| c2(I-)×c2(Fe3+) |
| c2(Fe2+)×c(I2) |
| c2(I-)×c2(Fe3+) |
[物质的浓度用“c(物质)”表示].当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡
(2)上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
| c(I-)(mol/L) | c(Fe3+)(mol/L) | v[mol/(L?s)] | |
| (1) | 0.20 | 0.80 | 0.032K |
| (2) | 0.60 | 0.40 | 0.144K |
| (3) | 0.80 | 0.20 | 0.128K |
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为
A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
②I-浓度对反应速率的影响
(1)各元素的符号:
A:______,B:______,C:______,D:______,X:______.
(2)写出C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序:______.
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:______.
ⅡFe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液),
(1)该反应的平衡常数K的表达式为:K=______.
[物质的浓度用“c(物质)”表示].当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡______移动(填“向右”、“向左”、“不”).
(2)上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
| c(I-)(mol/L) | c(Fe3+)(mol/L) | v[mol/(L?s)] | |
| (1) | 0.20 | 0.80 | 0.032K |
| (2) | 0.60 | 0.40 | 0.144K |
| (3) | 0.80 | 0.20 | 0.128K |
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为______.
A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
②I-浓度对反应速率的影响______Fe3+浓度对反应速率的影响(填“>”、“<”或“=”).
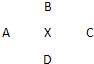
(1)各元素的符号:
A:______,B:______,C:______,D:______,X:______.
(2)写出C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序:______.
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:______.
ⅡFe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液),
(1)该反应的平衡常数K的表达式为:K=______.
[物质的浓度用“c(物质)”表示].当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡______移动(填“向右”、“向左”、“不”).
(2)上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
| c(I-)(mol/L) | c(Fe3+)(mol/L) | v[mol/] | |
| (1) | 0.20 | 0.80 | 0.032K |
| (2) | 0.60 | 0.40 | 0.144K |
| (3) | 0.80 | 0.20 | 0.128K |
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为______.
A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
②I-浓度对反应速率的影响______Fe3+浓度对反应速率的影响(填“>”、“<”或“=”).
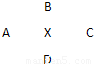 查看习题详情和答案>>
查看习题详情和答案>>
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为


(15分)
A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间在如图1所示的反应关系(反应物和生成物均无省略)。

请回答下列问题:
(1)图1所示转化过程中包含的反应类型有 (填字母)。
a.置换反应 b.复分解反应 c.分解反应 d.化合反应
(2)图1中反应①的化学方程式是 。(3分)
(3)图1中反应③在一定条件下为可逆反应,反应的能量变化如图2所示,当该反应处于平衡状态时,下列措施中有利于提高C的平衡转化率的是 (填字母)。
A.升高温度 B.降低温度 C.增大压强
D.减小压强 E.加入催化剂 F.增加C的量
(4)若将l.00 mol甲和2.00 mol C混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用甲表示的化学反应速率为
mol•L-1•min-1。
(5)容积均为2 L的四个密闭容器中均进行着(4)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
| 容器编号 | n(甲) | n(C) | n (D) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②? |
| Ⅲ | 0.60 | 1.20 | 0.80 | ③? |
①若方程式系数为最简整数比,则该温度下的平衡常数K=
填写表中空格: ② ③
查看习题详情和答案>>