摘要:18.甲烷在高温下与水蒸气反应.反应方程式为:CH4(g)+H2O+3H2(g).部分物质的燃烧热数据如下表: 物 质 燃烧热(kJ·mol-1) H2(g) -285.8 CO(g) -283.0 CH4(g) -890.3 已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量.写出CH4和H2O(g)在高温下反应的热化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_296851[举报]
甲烷在高温下与水蒸气反应,反应方程式为:CH4(g)+H2O(g)![]() CO(g)+3H2(g).部分物质的燃烧热数据如下表:
CO(g)+3H2(g).部分物质的燃烧热数据如下表:

已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量.写出CH4和H2O(g)在高温下反应的热化学方程式________.
 向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:I.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-802.6kJ/mol
II.CH4(g)+O2(g)═CO2(g)+2H2(g)△H2=-322.0kJ/mol
III.CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.2kJ/mol
Ⅳ.CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H4=+165.0kJ/mol
请回答下列问题:
(1)CH4的燃烧热△H
<
<
△H1.(填“>”、“<”或“=”).(2)在反应初始阶段,反应II的反应速率大于反应III的反应速率.比较反应II的活化能EII和反应III的活化能EIII的大小:EII
<
<
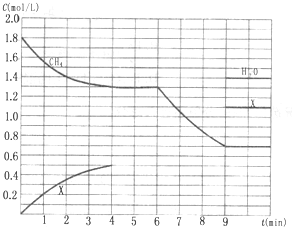
EIII(填“>”、“<”或“=”).(3)在1L固定容积密闭容器中投入1.8mol CH4和3.6mol H2O(g),若只发生反应Ⅳ,测得CH4、H2O(g)及某一生成物的物质的量浓度(c)随反应时间(t)的变化如图所示[第9min前H2O(g)的物质的量浓度及第4min~9min之间X所代表生成物的物质的量浓度变化曲线未标出,条件有变化时只考虑改变一个条件).
①0~4min内,H2的平均反应速率υ(H2)=
0.5
0.5
mol?(L?min)-1;②反应在5min时的平衡常数K=
0.91
0.91
;③第6min时改变的条件是
升高温度
升高温度
;判断理由是第6min~9min时的反应速率比0~4min时的大,且平衡向正反应方向移动,说明第6min改变的条件为升高温度或增加水蒸气的量,再根据第9min平衡时甲烷浓度为0.7mol/L,水蒸气浓度为1.4mol/L,说明甲烷消耗1.1mol,水蒸气消耗2.2mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度
第6min~9min时的反应速率比0~4min时的大,且平衡向正反应方向移动,说明第6min改变的条件为升高温度或增加水蒸气的量,再根据第9min平衡时甲烷浓度为0.7mol/L,水蒸气浓度为1.4mol/L,说明甲烷消耗1.1mol,水蒸气消耗2.2mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度
;④比较第5min时的平衡常数K5min与第10min时平衡常数K10min的大小:K5min
<
<
K10min (填“>”、“=”或“<”),原因是正反应为吸热反应,升高温度平衡常数增大
正反应为吸热反应,升高温度平衡常数增大
.运用所学的化学反应原理研究化学反应很有意义.请回答下列问题:
(1)合成氨原料中的H2可用甲烷在高温下与水蒸气反应制得.部分1mol物质完全燃烧生成常温下稳定氧化物的△H数据如下表:
已知1mol H2O(g)转变为1molH2O(l)时放热44.0kJ.写出CH4和水蒸气在高温下反应得到CO和H2的热化学方程式
(2)500°C、50Mpa时,在容积为VL的定容容器中加入n mol N2、3n mol H2,反应达到平衡后N2的转化率为a.则容器内气体的压强反应前与平衡时的比值为
.
(3)若把标准状况下4.48L氨气通入到100g19.6%的硫酸溶液中,所得溶液中的溶质是
(4)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.有沉淀析出的是
(5)以磷酸亚铁锂(LiFePO4)为电极材料的新型锂离子电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
查看习题详情和答案>>
(1)合成氨原料中的H2可用甲烷在高温下与水蒸气反应制得.部分1mol物质完全燃烧生成常温下稳定氧化物的△H数据如下表:
| 物质 | △H(kJ/mol) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.1kJ/mol
CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.1kJ/mol
.(2)500°C、50Mpa时,在容积为VL的定容容器中加入n mol N2、3n mol H2,反应达到平衡后N2的转化率为a.则容器内气体的压强反应前与平衡时的比值为
| 4n |
| 4n-2na |
| 4n |
| 4n-2na |
(3)若把标准状况下4.48L氨气通入到100g19.6%的硫酸溶液中,所得溶液中的溶质是
NH4HSO4
NH4HSO4
,溶液中离子浓度从大到小的顺序是c(H+)>c(SO42-)>c(NH+4)>c(OH-)
c(H+)>c(SO42-)>c(NH+4)>c(OH-)
.(4)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.有沉淀析出的是
b
b
点(填字母).a点对应的Ksp 
等于
等于
c点对应的Ksp (填大于、等于或小于)(5)以磷酸亚铁锂(LiFePO4)为电极材料的新型锂离子电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
FePO4+Li++e-═LiFePO4
FePO4+Li++e-═LiFePO4
.锆(?)主要用于核反应堆燃料棒的包层,这是因为含有1.5%Sn的锆合金具有在辐射下稳定的抗腐蚀性和机械性。以斜锆石(ZrO2)生产金属锆的生产过程示意图如下

(1) 写出斜锆石转化为四氯化锆的化学反应方程式:_____________________
(2) 已知:
①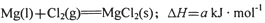
②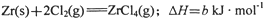
则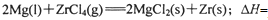 ______________ 该反应在Ar气氛中进行的理由是______________。
______________ 该反应在Ar气氛中进行的理由是______________。
(3) ZrCl4是白色固体,在潮湿的空气中“冒烟”。这是因为ZrCl4易发生_______反应,生成了 ______________。
(4) 2011年3月发生的日本福岛核电站爆炸,其原因是锆在高温下与水蒸气反应产生大量氢气,同时伴随着放热,最后氢气与空气混合发生爆炸。所发生的置换反应的化学方程式是_____________________
(5) —种新型燃料电池,一极通入空气,另一极通入甲烷;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-在熔融电解质中,O2-向_______ (填正、负)极移动。电池正极的电极反应式为_______,负极的电极反应式为___________。
查看习题详情和答案>>
(2) 已知:
①
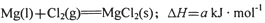
②
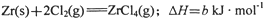
则
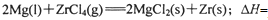 ______________ 该反应在Ar气氛中进行的理由是______________。
______________ 该反应在Ar气氛中进行的理由是______________。 (3) ZrCl4是白色固体,在潮湿的空气中“冒烟”。这是因为ZrCl4易发生_______反应,生成了 ______________。
(4) 2011年3月发生的日本福岛核电站爆炸,其原因是锆在高温下与水蒸气反应产生大量氢气,同时伴随着放热,最后氢气与空气混合发生爆炸。所发生的置换反应的化学方程式是_____________________
(5) —种新型燃料电池,一极通入空气,另一极通入甲烷;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-在熔融电解质中,O2-向_______ (填正、负)极移动。电池正极的电极反应式为_______,负极的电极反应式为___________。
运用所学的化学反应原理研究化学反应很有意义.请回答下列问题:
(1)合成氨原料中的H2可用甲烷在高温下与水蒸气反应制得.部分1mol物质完全燃烧生成常温下稳定氧化物的△H数据如下表:
已知1mol H2O(g)转变为1molH2O(l)时放热44.0kJ.写出CH4和水蒸气在高温下反应得到CO和H2的热化学方程式______.
(2)500°C、50Mpa时,在容积为VL的定容容器中加入n mol N2、3n mol H2,反应达到平衡后N2的转化率为a.则容器内气体的压强反应前与平衡时的比值为______.
(3)若把标准状况下4.48L氨气通入到100g19.6%的硫酸溶液中,所得溶液中的溶质是______,溶液中离子浓度从大到小的顺序是______.
(4)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.有沉淀析出的是______点(填字母).a点对应的Ksp ______c点对应的Ksp (填大于、等于或小于)
(5)以磷酸亚铁锂(LiFePO4)为电极材料的新型锂离子电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)合成氨原料中的H2可用甲烷在高温下与水蒸气反应制得.部分1mol物质完全燃烧生成常温下稳定氧化物的△H数据如下表:
| 物质 | △H(kJ/mol) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
(2)500°C、50Mpa时,在容积为VL的定容容器中加入n mol N2、3n mol H2,反应达到平衡后N2的转化率为a.则容器内气体的压强反应前与平衡时的比值为______.
(3)若把标准状况下4.48L氨气通入到100g19.6%的硫酸溶液中,所得溶液中的溶质是______,溶液中离子浓度从大到小的顺序是______.
(4)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.有沉淀析出的是______点(填字母).a点对应的Ksp ______c点对应的Ksp (填大于、等于或小于)
(5)以磷酸亚铁锂(LiFePO4)为电极材料的新型锂离子电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为______.
 查看习题详情和答案>>
查看习题详情和答案>>