摘要: [实验探究] 稀盐酸.硫酸铜等,冒气泡.出现红色固体等 [理论探讨] l535℃-l538℃ Fe2O3 Fe3O4 [拓展延伸](1) 在集气瓶底部放少量的水(或在集气瓶底部铺一层细沙) (2) 由黑色变成红棕色 (3) A>C>B
网址:http://m.1010jiajiao.com/timu3_id_29546[举报]
(2010?葫芦岛)学习中和反应后,老师做了如下实验:在烧杯中加入40g氢氧化钠溶液,滴入几滴酚酞溶液,再向烧杯中加入36,5g稀盐酸,振荡,溶液由红色变成无色.老师让同学们对实验中稀盐酸和氢氧化钠溶液是否完全反
应进行探究.请你和同学们-起完成实验.
【做出猜想】
猜想一:恰好完全反应;
猜想二:稀盐酸有剩余;
猜想三:氢氧化钠有剩余.
【交流表达】
(1)反应的化学方程式为
(2)同学们讨论后,认为猜想三不成立.理由是:
查看习题详情和答案>>
应进行探究.请你和同学们-起完成实验.
【做出猜想】
猜想一:恰好完全反应;
猜想二:稀盐酸有剩余;
猜想三:氢氧化钠有剩余.
【交流表达】
(1)反应的化学方程式为
Na0H+HCl═NaCl+H2O
Na0H+HCl═NaCl+H2O
.(2)同学们讨论后,认为猜想三不成立.理由是:
酚酞在碱性溶液中显红色,反应后溶液为无色,所以不含氢氧化钠
酚酞在碱性溶液中显红色,反应后溶液为无色,所以不含氢氧化钠
.23、实验是学习化学的重要途径.下面是小刚同学设计的几个实验:①稀盐酸与石蕊反应②铝与稀盐酸反应③氧化铜与稀盐酸反应④氢氧化钠与稀盐酸反应⑤碳酸钠与稀盐酸反应,请回答下列问题:
(1)小刚的实验目的是
(2)第三个实验的现象是
(3)小刚将④⑤两个实验的废液混合,取少量向其中滴入少量酚酞试液,溶液变为红色,则该溶液中一定含有的溶质是
查看习题详情和答案>>
(1)小刚的实验目的是
探究盐酸的化学性质
(2)第三个实验的现象是
黑色粉末逐渐溶解,溶液由无色变成蓝色
(3)小刚将④⑤两个实验的废液混合,取少量向其中滴入少量酚酞试液,溶液变为红色,则该溶液中一定含有的溶质是
NaCl,
可能含有的溶质是Na2CO3和NaOH中的一种或两种
,为了证明该溶液的组成,小刚做了如下实验,请你帮他完成| 实验步骤 | 实验现象 | 实验结论 |
| a、取少量混合溶液于试管中向里滴加足量的 氯化钙溶液 |
有白色沉淀生成 |
该溶液的溶质是 氯化钠、碳酸钠和氢氧化钠 |
| b、继续向里滴加 酚酞试液 |
溶液变成红色 |
氢氧化钠是一种重要的化工原料,工业上常用电解饱和食盐水的方法来制取烧碱、氯气(Cl2)和氢气.
(1)写出工业上电解饱和食盐水的化学方程式 .
(2)盛氢氧化钠溶液的试剂瓶口可能会出现白色的碳酸钠粉末,用化学方程式表示其原理.如何证实白色粉末中含有碳酸钠?
(3)为了探究NaOH和CO2确实发生了化学反应,某实验小组的同学设计出了下列4种实验装置,请回答下列问题:
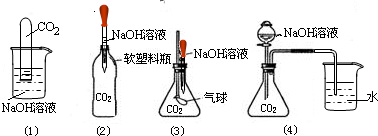
选择任意一种实验装置,简述出现的实验现象,解释产生该实验现象的原因.
选择的实验装置是装置 (填序号).
实验现象为: .
产生该实验现象的原因是: .
(4)稀盐酸和氢氧化钠溶液发生复分解反应时,无明显的现象,设计实验证明稀盐酸和氢氧化钠溶液发生了反应.
(5)有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加一定溶质质量分数的稀盐酸,放出气体的质量为0.88g.试求:样品中氢氧化钠的质量分数是多少? 查看习题详情和答案>>
(1)写出工业上电解饱和食盐水的化学方程式
(2)盛氢氧化钠溶液的试剂瓶口可能会出现白色的碳酸钠粉末,用化学方程式表示其原理.如何证实白色粉末中含有碳酸钠?
(3)为了探究NaOH和CO2确实发生了化学反应,某实验小组的同学设计出了下列4种实验装置,请回答下列问题:

选择任意一种实验装置,简述出现的实验现象,解释产生该实验现象的原因.
选择的实验装置是装置
实验现象为:
产生该实验现象的原因是:
(4)稀盐酸和氢氧化钠溶液发生复分解反应时,无明显的现象,设计实验证明稀盐酸和氢氧化钠溶液发生了反应.
(5)有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加一定溶质质量分数的稀盐酸,放出气体的质量为0.88g.试求:样品中氢氧化钠的质量分数是多少? 查看习题详情和答案>>
30、用盐酸可以清除铁锈(主要成分为Fe2O3),盐酸中主要含有H2O分子、H+、C1一.某探究小组为探究稀盐酸中的哪种微粒能使氧化铁溶解:设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
(2)是否需要做“向Fe2O3中加入水”的对比实验?为什么?
(3)写出发生反应的化学方程式.
查看习题详情和答案>>
(1)请填写下表中的实验结论:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量Fe2O3的试管中 加入NaCl溶液振荡 |
固体不溶解 | Cl-不能使Fe2O3溶解,H2O不能使Fe2O3溶解 |
(3)写出发生反应的化学方程式.
 26、生活中我们经常发现存放的铁钉会生锈.
26、生活中我们经常发现存放的铁钉会生锈.(1)小牛和小明通过如图所示实验对铁制品生锈的条件进行探究.通过观察和分析:
最易生锈的是
A
(填序号),试管B中加入植物油的目的是隔绝空气
.我得出铁生锈的条件是与氧气、水同时接触(或在潮湿的空气中)
.(2)在实验室用稀盐酸除铁锈的实验中,小牛认为盐酸中含有H2O、H+、Cl-三种粒子,为了探究稀盐酸中哪种粒子能使铁锈溶解,他进行了如下实验,我能帮他完成.

小明认为还需要补做一个“向装有锈铁钉的试管中加入水”的对比实验,我认为这个实验是多余的,理由是
NaCl溶液中含有H2O
.小明在做铁钉除锈实验时,由于忘了及时从稀盐酸中取出已除掉铁锈的铁钉,过了一段时间后,他发现铁钉表面居然出现了黑色物质.通过分析我认为铁钉表面的黑色物质可能是
炭(或“C”)
.(3)为了探究铁锈除掉后溶液的组成,小牛将生锈的铁钉放入一支试管中,加入一定量的稀盐酸,待铁钉表面的铁锈恰好溶解完时,迅速取出铁钉,再进行以下实验.

我能写出(3)中的一个化学方程式
Fe+2FeCl3═3FeCl2或Fe2O3+6HCl═2FeCl3+3H2O或Fe+2HCl═FeCl2+H2↑
.(4)通过以上探究,我获得的启示是
在干燥的环境中,铁制品不易生锈;给金属除锈时,不能长时间将金属浸在酸中;铁钉是铁合金;
.