摘要:5.在2mL物质的量浓度相等的NaCl和NaI混合溶液中滴入几滴AgNO3溶液.发生的反应为 A.只有AgCl沉淀生成 B.只有AgI沉淀生成 C.生成等物质的量的AgCl和AgI沉淀 D.两种沉淀都有.但以AgI为主
网址:http://m.1010jiajiao.com/timu3_id_294566[举报]
在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO3溶液,发生的反应为.
A.只有AgCl沉淀生成 B.只有AgI沉淀生成
C.生成等物质的量的AgCl和AgI沉淀 D.两种沉淀都有,但以AgI为主
查看习题详情和答案>>下述实验能达到预期目的是( )
查看习题详情和答案>>
| 编号 | 实验内容 | 实验目的 |
| A | 取两只试管,分别加入4mL 0.01mol/L KMnO4酸性溶液,然后向一只试管中加入0.1mol/L H2C2O4溶液2mL,向另一只试管中加入0.1mol/L H2C2O4溶液 4mL,记录褪色时间 |
证明草酸浓度越大反应速率越快 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向1mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,溶解度Mg(OH)2>Fe(OH)3 |
| D | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
(1)下列实验中所选用的仪器合理的是
A.用200mL量筒量取5.2mL稀H2SO4
B.用100mL烧杯配制100g质量分数为1%的食盐水
C.用托盘天平称取11.7gNaCl晶体
D.用碱式滴定管量取25.1mL溴水
E.用250mL容量瓶配制250mL0.20mol/L的氢氧化钠溶液
(2)下列实验操作是不正确的,请将这些操作可能发生的不良后果填在空白中.
A.给试管中的液体加热时,液体超过试管容积的
B.用碱式滴定管盛装KMnO4溶液
(3)配制一定物质的量浓度的溶液时
①所必须的仪器为
②若定容时俯视,所配溶液的物质的量浓度比要求的值
③若定容后摇匀静置,发现凹液面低于刻度线,此时应该(填标号)
A.直接转移到试剂瓶中
B.加水重新定容后贮存于容量瓶中
C.重新定容后再转移到试剂瓶中.
查看习题详情和答案>>
C、E
C、E
A.用200mL量筒量取5.2mL稀H2SO4
B.用100mL烧杯配制100g质量分数为1%的食盐水
C.用托盘天平称取11.7gNaCl晶体
D.用碱式滴定管量取25.1mL溴水
E.用250mL容量瓶配制250mL0.20mol/L的氢氧化钠溶液
(2)下列实验操作是不正确的,请将这些操作可能发生的不良后果填在空白中.
A.给试管中的液体加热时,液体超过试管容积的
| 1 | 3 |
液体沸腾时易冲出试管
液体沸腾时易冲出试管
.B.用碱式滴定管盛装KMnO4溶液
碱式滴定管的橡胶管可被腐蚀,滴定管漏水
碱式滴定管的橡胶管可被腐蚀,滴定管漏水
.(3)配制一定物质的量浓度的溶液时
①所必须的仪器为
量筒(或托盘天平)、烧杯、玻璃棒、容量瓶、胶头滴管
量筒(或托盘天平)、烧杯、玻璃棒、容量瓶、胶头滴管
②若定容时俯视,所配溶液的物质的量浓度比要求的值
偏高
偏高
(填“偏高”或“偏低”)③若定容后摇匀静置,发现凹液面低于刻度线,此时应该(填标号)
A
A
A.直接转移到试剂瓶中
B.加水重新定容后贮存于容量瓶中
C.重新定容后再转移到试剂瓶中.
实验:
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: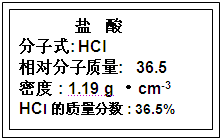
①该浓盐酸中HCl的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
B.忘记将洗涤液加入容量瓶
C.容量瓶内壁附有水珠而未干燥处理
D.溶解后没有冷却便进行定容
(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
查看习题详情和答案>>
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

①该浓盐酸中HCl的物质的量浓度为
11.9
11.9
mol?L-1.②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是BD
BD
.A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
11.4
11.4
g②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
10.6
10.6
g(1g以下用游码)③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
B
B
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
偏低
偏低
;B.忘记将洗涤液加入容量瓶
偏低
偏低
;C.容量瓶内壁附有水珠而未干燥处理
不变
不变
;D.溶解后没有冷却便进行定容
偏高
偏高
.(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
,反应后得到黄色的FeCl3溶液.用此溶液做以下实验:②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
Fe3++3O H-=Fe(OH)3↓
Fe3++3O H-=Fe(OH)3↓
.③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
红褐
红褐
色,即可制得Fe(OH)3胶体.④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
乙
乙
(填甲或乙)烧杯中会产生丁达尔效应.此实验可以区别溶液和胶体
溶液和胶体
.(1)只用一种试剂区别Na2SO4、MgCl2、FeCl3、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是
(2)如果a g某气体中含有的分子数为b,则c g 该气体在标准状况下的体积约是
L
L
(3)已知6L Al2(SO4)3溶液中含有Al3+为0.6mol,则Al2(SO4)3溶液的物质的量浓度为
(4)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为
查看习题详情和答案>>
NaOH溶液
NaOH溶液
(2)如果a g某气体中含有的分子数为b,则c g 该气体在标准状况下的体积约是
| 22.4bc |
| aNA |
| 22.4bc |
| aNA |
(3)已知6L Al2(SO4)3溶液中含有Al3+为0.6mol,则Al2(SO4)3溶液的物质的量浓度为
0.05
0.05
mol/L,取上述溶液2ml加水稀释到10ml,此溶液中SO42-的物质的量浓度为0.03
0.03
mol/L.(4)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为
A-N-2
A-N-2
.