网址:http://m.1010jiajiao.com/timu3_id_288057[举报]
 实验室制备乙酸正丁酯的化学方程式:
实验室制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
制备过程中还可能的副反应有:
CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
主要实验步骤如下:
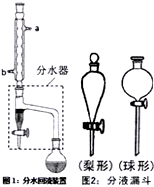
①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器、冷凝管.然后小火加热.
②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥.④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数:
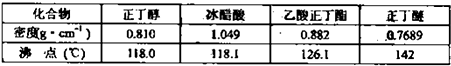
根据以上信息回答下列问题.
(1)图1装置中冷水应从
(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是
A.实验室沸石也可用碎瓷片等代替 B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用 D.沸石为多孔性物质,可使液体平稳地沸腾
(3)在步骤③分液时,分液漏斗旋塞的操作方法与酸式滴定管的是否相同
(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质
(5)步骤④的常压蒸馏,需收集
实验室用铜制备CuSO4溶液有多种方案,某实验小组给出了以下三种方案: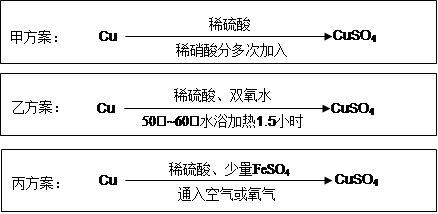
请回答有关问题:
(1)甲方案:
①写出该反应的离子方程式 ;
②为了节约原料,硫酸和硝酸的物质的量之比最佳为,n(H2SO4):n(HNO3)= 。
(2)乙方案:将6.4g铜丝放到90mL 1.5mol·L-1的稀硫酸中,控温在50℃。加入40mL 10%的H2O2,反应0.5小时,升温到60℃,持续反应1小时后,经一系列操作,得CuSO4·5H2O 20.0g【已知有关摩尔质 量:M(Cu)=64g/mol, M(CuSO4·5H2O) =250g/mol】。
①反应时温度控制在50℃~60℃,不宜过高的原因是 ;
②本实验CuSO4·5H2O的产率为 。
(3)丙方案:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质A调节pH至4 ,然后过滤、浓缩、结晶。
①物质A可选用以下的 (填序号);
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
(4)对比甲、乙、丙三种实验方案,丙方案的优点有(写两条):
、 。 查看习题详情和答案>>
实验室常用铜片、稀硫酸和浓硝酸来制备五水硫酸铜:Cu+2HNO3+H2SO4=CuSO4+2NO2↑+2H2O分以下几个步骤:
①将盛有4.5g铜屑的蒸发皿置于酒精灯火焰上,灼烧至表面呈现黑色,冷却;
②加16mL3mol?L-1硫酸,再缓慢、分批加入7mL12mol?L-1硝酸(在通风橱进行);
③待反应缓和后,盖上表面皿,用水浴加热至铜屑全溶;
④倾析法趁热将溶液转移到另一蒸发皿中,并在水浴上浓缩到溶液出现晶膜,冷却,过滤;
…
请回答下列问题:
(1)将铜屑灼烧的目的是______,表面的黑色物质是______.
(2)加入硝酸时,必须缓慢、分批加入的目的是______.
(3)控制硝酸总量尽可能小除了环保和节约原料外,还可能的原因是______.
(4)下图是硫酸铜和硝酸铜的溶解度表(单位:g),请根据表回答:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4?5H2O | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| Cu(NO3)2?xH2O | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
②将五水硫酸铜粗产品提纯,要采取的实验方法是______.
(5)实验中取用蒸发皿的仪器是______,使用蒸发皿时的注意事项是______.(只需写出一项)
(6)如不用水浴加热蒸发,五水硫酸铜晶体可能会因温度高转变为白色的硫酸铜,此过程属于______变化.(填“物理”或“化学”) 查看习题详情和答案>>
①将盛有4.5g铜屑的蒸发皿置于酒精灯火焰上,灼烧至表面呈现黑色,冷却;
②加16mL3mol?L-1硫酸,再缓慢、分批加入7mL12mol?L-1硝酸(在通风橱进行);
③待反应缓和后,盖上表面皿,用水浴加热至铜屑全溶;
④倾析法趁热将溶液转移到另一蒸发皿中,并在水浴上浓缩到溶液出现晶膜,冷却,过滤;
…
请回答下列问题:
(1)将铜屑灼烧的目的是______,表面的黑色物质是______.
(2)加入硝酸时,必须缓慢、分批加入的目的是______.
(3)控制硝酸总量尽可能小除了环保和节约原料外,还可能的原因是______.
(4)下图是硫酸铜和硝酸铜的溶解度表(单位:g),请根据表回答:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4?5H2O | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| Cu(NO3)2?xH2O | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
②将五水硫酸铜粗产品提纯,要采取的实验方法是______.
(5)实验中取用蒸发皿的仪器是______,使用蒸发皿时的注意事项是______.(只需写出一项)
(6)如不用水浴加热蒸发,五水硫酸铜晶体可能会因温度高转变为白色的硫酸铜,此过程属于______变化.(填“物理”或“化学”)
实验室常用铜片、稀硫酸和浓硝酸来制备五水硫酸铜:
Cu + 2HNO3 + H2SO4 = CuSO4 +2NO2↑+2H2O
分以下几个步骤:
①将4.5g铜屑的蒸发皿置于酒精灯火焰上,灼烧至表面呈现黑色,冷却;
②加16mL3mol?L-1硫酸,再缓慢、分批加入7mL 12mol?L-1硝酸(在通风橱进行);
③待反应缓和后,盖上表面皿,用水浴加热至铜屑全溶;
④倾析法趁热将溶液转移到另一蒸发皿中,并在水浴上浓缩到溶液出现少量晶体,冷却,过滤;
请回答下列问题:
(1)将铜屑灼烧,表面的黑色物质是 。
(2)加入硝酸时,必须缓慢、分批加入的目的是 。
(3)下图是硫酸铜和硝酸的溶解度表(单位:g),请根据表回答:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4?5H2O | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| Cu(NO3)2?Xh2O | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
①步骤④溶液冷却时析出的晶体主要是 。
②将所得晶体的粗产品提纯,通常采取的实验方法是 。
(4)实验中取用蒸发皿的仪器是 ,使用蒸发皿时的注意事项是 。(只需写出一项)
(5)步骤④中若不用水浴加热蒸发,所得晶体可能会因温度高转变为白色的粉末,此过程属于 变化。(填“物理”或“化学”)
查看习题详情和答案>>