题目内容
 实验室制备乙酸正丁酯的化学方程式:
实验室制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
制备过程中还可能的副反应有:
CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
主要实验步骤如下:
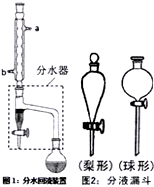
①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器、冷凝管.然后小火加热.
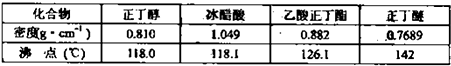
②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥.④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数:
根据以上信息回答下列问题.
(1)图1装置中冷水应从
(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是
A.实验室沸石也可用碎瓷片等代替 B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用 D.沸石为多孔性物质,可使液体平稳地沸腾
(3)在步骤③分液时,分液漏斗旋塞的操作方法与酸式滴定管的是否相同
(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质
(5)步骤④的常压蒸馏,需收集
分析:(1)冷水从下进上出;水的密度较大;除掉生成物平衡右移;
(2)沸石为多孔性物质,可用碎瓷片等代替;
(3)当酸式滴定管的刻度面面对操作者时,一般用左手控制滴定管旋塞而右手摇动锥形瓶.而分液漏斗不存在也不需要读刻度,可用右手操作,左手扶住;梨形分液漏斗靠近旋塞处比较细长;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液;酯在碱性条件下能发生水解;
(5)乙酸正丁酯的沸点是126.1度;水冷凝管温度较低.
(2)沸石为多孔性物质,可用碎瓷片等代替;
(3)当酸式滴定管的刻度面面对操作者时,一般用左手控制滴定管旋塞而右手摇动锥形瓶.而分液漏斗不存在也不需要读刻度,可用右手操作,左手扶住;梨形分液漏斗靠近旋塞处比较细长;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液;酯在碱性条件下能发生水解;
(5)乙酸正丁酯的沸点是126.1度;水冷凝管温度较低.
解答:解:(1)冷水从下进上出冷凝效果最好;水的密度比乙酸正丁酯大;将水分离使平衡正向移动,提高反应产率,故答案为:b;水;分离酯化反应生成的水,使平衡正向移动,提高反应产率;
(2)A.沸石为多孔性物质,可用碎瓷片等代替,故A正确; B.如果忘加沸石,将沸石加至将近沸腾的液体中,可能引起液体飞溅,故B错误;
C.使用过一次后,空气几乎排尽,被液体填充,不再具有提供汽化中心的效果,故C错误;
D.沸石的工作原理是提供汽化中心,汽化中心的来源是沸石多孔结构中包含的空气.这些空气在加热后膨胀,形成气泡溢出,成为了汽化中心,故D正确.
故选AD;
(3)当酸式滴定管的刻度面面对操作者时,下端的出液控制旋塞的旋柄在操作者的右边(旋塞是从右往左 放进去的),操作者既要用手的手指轻轻推动旋塞柄 缓慢放溶液,又要保证旋塞不被从旋塞体内拔出而漏溶液造成滴定失败,因此手指有一个既推动旋塞 又向左拉住旋塞芯的微小的力量,所以一般用左手控制滴定管旋塞而右手摇动锥形瓶.而分液漏斗不存在也不需要读刻度,可用右手操作,左手扶住;梨形分液漏斗靠近旋塞处比较细长,分离操作更容易,
故答案为:不相同;梨;梨形分液漏斗靠近旋塞处比较细长,双液界面更清晰,分离更完全;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液,且乙酸正丁酯在碳酸钠溶液的溶解度较小;乙酸正丁酯在碱性条件下能发生水解,故答案为:乙酸、硫酸、正丁醇;不可以;用氢氧化钠溶液会使乙酸正丁酯发生水解;
(5)乙酸正丁酯的沸点是126.1度,需收集126℃左右的馏分;水冷凝管温度较低,温差过大,冷凝管会炸裂,故答案为:126度;防止因温差过大,冷凝管炸裂.
(2)A.沸石为多孔性物质,可用碎瓷片等代替,故A正确; B.如果忘加沸石,将沸石加至将近沸腾的液体中,可能引起液体飞溅,故B错误;
C.使用过一次后,空气几乎排尽,被液体填充,不再具有提供汽化中心的效果,故C错误;
D.沸石的工作原理是提供汽化中心,汽化中心的来源是沸石多孔结构中包含的空气.这些空气在加热后膨胀,形成气泡溢出,成为了汽化中心,故D正确.
故选AD;
(3)当酸式滴定管的刻度面面对操作者时,下端的出液控制旋塞的旋柄在操作者的右边(旋塞是从右往左 放进去的),操作者既要用手的手指轻轻推动旋塞柄 缓慢放溶液,又要保证旋塞不被从旋塞体内拔出而漏溶液造成滴定失败,因此手指有一个既推动旋塞 又向左拉住旋塞芯的微小的力量,所以一般用左手控制滴定管旋塞而右手摇动锥形瓶.而分液漏斗不存在也不需要读刻度,可用右手操作,左手扶住;梨形分液漏斗靠近旋塞处比较细长,分离操作更容易,
故答案为:不相同;梨;梨形分液漏斗靠近旋塞处比较细长,双液界面更清晰,分离更完全;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液,且乙酸正丁酯在碳酸钠溶液的溶解度较小;乙酸正丁酯在碱性条件下能发生水解,故答案为:乙酸、硫酸、正丁醇;不可以;用氢氧化钠溶液会使乙酸正丁酯发生水解;
(5)乙酸正丁酯的沸点是126.1度,需收集126℃左右的馏分;水冷凝管温度较低,温差过大,冷凝管会炸裂,故答案为:126度;防止因温差过大,冷凝管炸裂.
点评:本题考查酯的制取和性质实验,难度不大,注意分液漏斗不存在也不需要读刻度.

练习册系列答案
相关题目
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的物理性质如下表。请回答有关问题。
|
化合物 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100 g水 |
|
正丁醇 |
0.810 |
118.0 |
9 |
|
冰醋酸 |
1.049 |
118.1 |
∞ |
|
乙酸正丁酯 |
0.882 |
126.1 |
0.7 |
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50 mL圆底烧瓶中,装入沸石,加入11.5 mL正丁醇和9.4 mL冰醋酸,再加3~4滴浓硫酸。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应。
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:______________、______________。
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是________________、________________。
Ⅱ.乙酸正丁酯精产品的制备
(1)将乙酸正丁酯粗产品用如下操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠溶液洗涤,正确的操作步骤是__________(填字母)。
A.①②③④ B.③①④②
C.①④①③② D.④①③②③
(2)将酯层采用如下图所示装置蒸馏。
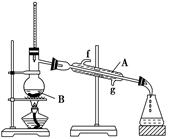
①写出上图中仪器A的名称______________,冷却水从__________口进入(填字母)。
②蒸馏收集乙酸正丁酯产品时,应将温度控制在__________左右。
Ⅲ.计算产率
测量分水器内由乙酸与正丁醇反应生成水的体积为1.8 mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率为__________。

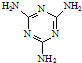 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 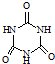 )后,三聚氰酸与三聚氰胺分子相互之间通过
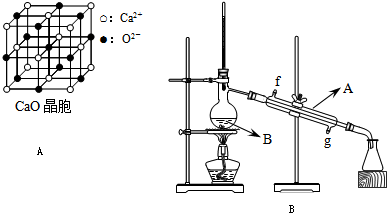
)后,三聚氰酸与三聚氰胺分子相互之间通过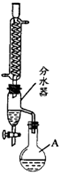 (2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
(2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下: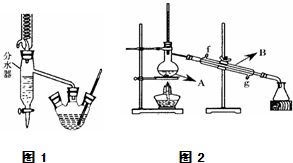 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.