摘要:25.已知A-H是中学化学中的常见物质.A.C.G是金属.E.F是氧化物.B溶于水得蓝色溶液.它们有如下图所示的关系. 试回答下列问题. (1)推断填写物质化学式:A是 ▲ .D是 ▲ .H是 ▲ . (2)F的类别是 ▲ (选填“酸性氧化物 .“碱性氧化物 或“两性氧化物 ). (3)反应④的化学方程式为 ▲ .
网址:http://m.1010jiajiao.com/timu3_id_281736[举报]
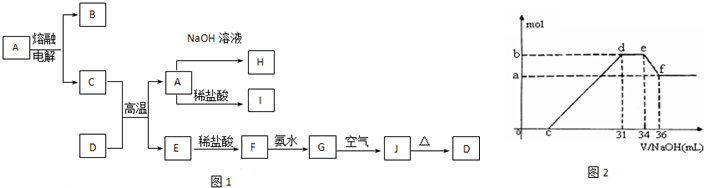
A-J是中学化学中常见的物质,它们之间的转化关系如框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.请回答下列问题:
(1)A的化学式为
(2)H溶液中通入过量的CO2,其反应的离子方程式是
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
上述现象说明溶液中
③b与a的差值为
查看习题详情和答案>>
(1)A的化学式为
Al2O3
Al2O3
(2)H溶液中通入过量的CO2,其反应的离子方程式是
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
G→J的化学方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
4Fe(OH)2+2H2O+O2═4Fe(OH)3
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
H++OH-=H2O
H++OH-=H2O
.②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
;上述现象说明溶液中
H+
H+
结合OHˉ的能力最强(填离子符号).③b与a的差值为
0.008mol
0.008mol
mol.
 A-K是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,G、H为气态单质,I在常温下为液体,D、E、F的水溶液均呈碱性,由C的饱和溶液制取F或E是重要的化工生产.回答下列问题:
A-K是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,G、H为气态单质,I在常温下为液体,D、E、F的水溶液均呈碱性,由C的饱和溶液制取F或E是重要的化工生产.回答下列问题:(1)写出下列物质的化学式:C
NaCl
NaCl
ENaHCO3
NaHCO3
(2)写出下列反应的化学方程式:
B→D:
2Na202+2C02=2Na2CO3+02
2Na202+2C02=2Na2CO3+02
C→E:
NaCl+NH3+C02+H2O=NaHCO3↓+NH4Cl
NaCl+NH3+C02+H2O=NaHCO3↓+NH4Cl
(3)画出F的电子式:


(4)常温下若电解1L C的饱和溶液,当电路中通过0.1mol电子时,溶液的pH值(假设溶液体积不变)为
13
13
.A-J是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂.
(1)写出E的电子式:
 .
.
(2)写出反应⑦的离子方程式:
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:
查看习题详情和答案>>
(1)写出E的电子式:


(2)写出反应⑦的离子方程式:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:
4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
.(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:
2Cl--2e-=Cl2
2Cl--2e-=Cl2
.
A-J是中学化学中常见的物质,它们之间的转化关系如下框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.

请回答下列问题:
(1)A的化学式为 .
(2)H与I溶液混合后,发生反应的离子方程式是 .G→J的化学方程式为 .
(3)D物质恰好溶于一定量的稀盐酸后,所得溶液显酸性的原因(用方程式表示) .
(4)实验证明,硝酸发生氧化还原反应时,硝酸越稀对应还原产物中氮元素的化合价越低.某同学取一定量的C、E合金与一定量的很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入一定浓度的氢氧化钠溶液,所加氢氧化钠的物质的量与产生的沉淀的物质的量(mol)的关系如图2所示.试回答下列问题:
①图2中OC段没有沉淀生成,此阶段发生的离子方程式为: .
②在DE段没有沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为: ;
③B点对应的沉淀量为 mol,C点对应的横坐标为 mol.
查看习题详情和答案>>

请回答下列问题:
(1)A的化学式为
(2)H与I溶液混合后,发生反应的离子方程式是
(3)D物质恰好溶于一定量的稀盐酸后,所得溶液显酸性的原因(用方程式表示)
(4)实验证明,硝酸发生氧化还原反应时,硝酸越稀对应还原产物中氮元素的化合价越低.某同学取一定量的C、E合金与一定量的很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入一定浓度的氢氧化钠溶液,所加氢氧化钠的物质的量与产生的沉淀的物质的量(mol)的关系如图2所示.试回答下列问题:
①图2中OC段没有沉淀生成,此阶段发生的离子方程式为:
②在DE段没有沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为:
③B点对应的沉淀量为
A—J是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂。
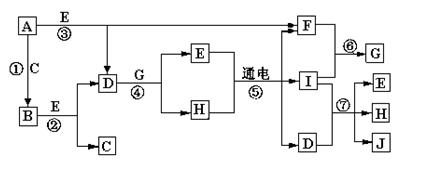
回答下列问题:
(1)B的化学式: ,E的电子式_________。
(2)写出反应⑦的离子方程式 __________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式_____________________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则在_____________(填“阴、阳”)极附近溶液由无色变为红色,其原因是_________________ 。
查看习题详情和答案>>