摘要:2.碳酸铵在室温下就能自发分解产生氨气.下列有关认识正确的是 A.碳酸铵分解是因为生成了易挥发的气体.使体系的熵增大 B.碳酸铵分解是因为外界给予了能量 C.碳酸铵分解是吸热反应.根据焓判据不能自发分解 D.碳酸盐都不稳定.都能自发分解
网址:http://m.1010jiajiao.com/timu3_id_279234[举报]
下列表述不正确的是
| A.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
| B.铝热反应会放出大量的热,因此常温下就能顺利发生 |
| C.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
D.对于化学反应COCl2(g) CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 |
下列表述不正确的是
A.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大
B.铝热反应会放出大量的热,因此常温下就能顺利发生
C.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
D.对于化学反应COCl2(g)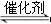 CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率
CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率
查看习题详情和答案>>
下列表述不正确的是
| A.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
| B.铝热反应会放出大量的热,因此常温下就能顺利发生 |
| C.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
D.对于化学反应COCl2(g) CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 |