摘要:1.H-可与NH3发生如下反应:H-+NH3NH2-+H2.据此可以说明 A.NH3具有还原性 B.H-作还原剂 C.该反应是置换反应 D.该反应不是氧化还原反应
网址:http://m.1010jiajiao.com/timu3_id_278004[举报]
 (2009?合肥三模)A、B、C、D、E是中学常见的单质,X是化合物.A为金属,原子最外层p轨道上只有一个电子,可与NaOH溶液反应;B是常见的金属,其基态原子的外围电子排布式为3d64s2;常温下C是气态非金属单质,可以燃烧;D是空气主要成分之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:
(2009?合肥三模)A、B、C、D、E是中学常见的单质,X是化合物.A为金属,原子最外层p轨道上只有一个电子,可与NaOH溶液反应;B是常见的金属,其基态原子的外围电子排布式为3d64s2;常温下C是气态非金属单质,可以燃烧;D是空气主要成分之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:(1)写出单质B与Cl2的反应产物与X的水溶液反应的离子方程式:
Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+
Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+
.B单质在海水中易发生电化学腐蚀,写出电化学腐蚀的正极电极方程式:O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
.(2)已知单质E的燃烧热为296.8kJ/mol,写出表示E燃烧热的热化学方程式:
S(g)+O2(g)═SO2(g);△H=-296.8kJ/mol
S(g)+O2(g)═SO2(g);△H=-296.8kJ/mol
.(3)写出A的氧化物与NaOH溶液反应的离子方程式:
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
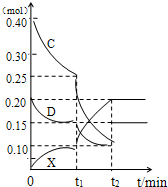
.(4)将0.40molC和0.20molD充入2L的密闭容器中,在一定条件下反应生成X,有关C、D、X三者的物质的量的变化与时间的关系如图所示:
①若t1=10min 则0~t1时间内C物质的平均反应速率为
0.0075mol/(L?min)
0.0075mol/(L?min)
;该反应平衡常数表达式为| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
②该反应在t2时达到平衡,根据图中曲线变化情况判断,t1时刻改变的反应条件可能是
a
a
(填序号)a.加入了催化剂 b.降低了反应温度 c.向容器中又充入了气体D.
硅——无机非金属材料的主角.未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是化合物G.
(1)化合物G的相对分子质量为140,G为两种元素组成的化合物,其中硅元素的质量分数为60%,另一种元素为空气中含量最高的元素Y.
①化合物G的化学式为________,
②G可以由四氯化硅与NH3在反应而生成,同时产生HCl气体.写出反应方程式________
(2)粉末状G在高温下可与水发生反应,写出其反应方程式________;
(3)水泥是重要的无机非金属材料之一,普通水泥在固化过程中自由水分子减少并形成碱性溶液.根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是________
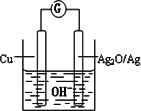
A.工业上以黏土、石灰石和石英为主要原料来制造普通水泥
B.负极的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O
C.测量原理示意图中,电流方向从Cu→Ag2O
D.电池工作时,OH-向正极移动
(4)已知粗硅提纯,总反应式可用表示为:
SiCl4(g)+2H2(g) Si(s)+4HCl(g),ΔH=+236 kJ·mol-1下表是部分化学键的键能数据:
则上表中x=________.
 氨气在化肥、致冷剂、有机合成工业中都有广泛应用.
氨气在化肥、致冷剂、有机合成工业中都有广泛应用.(1)实验室制取氨气的化学方程式为
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应也可生成氨气.
已知:①2N2(g)+6H2O(l)═4NH3(g)+3O2(g)△H1=2akJ?mol-1
②N2(g)+3H2(g)═2NH3(g)△H2=-92.4kJ?mol-1
③2H2(g)+O2(g)=2H2O(l)△H3=-571.6kJ?mol-1
则a=
765
765
.(3)N2+3H2
| 催化剂 |
| 高温高压 |
②④
②④
.①该反应的K=c(N2)?c3(H2)/c2(NH3) ②2υ正(H2)=3υ逆(NH3) ③改变条件,N2、H2、NH3的浓度可能会变化,K值也会随之变化 ④每有3molH-H键断裂,同时一定有6molN-H键断裂
(4)在一容积为2L的密闭容器中,加入0.2mol N2和0.6mol H2,在一定条件下发生如下反应:N2(g)+3H2(g)═2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如图所示.
结合如图计算从反应开始到平衡时,用NH3表示的平均反应速率υ(NH3)=
0.025mol/(L?min)
0.025mol/(L?min)
.反应到平衡时N2的转化率为50%
50%
.已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质;Y在常温下为液态,E的相对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去):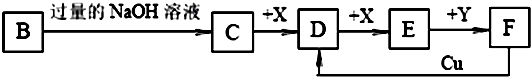
请回答下列问题:
(1)B的化学式为 ;F与Cu反应的离子方程式为_ ;
(2)C可与过量的Cl2 反应生成HCl和物质A,A可发生水解反应生成NH3和HClO,则C与过量Cl2反应的化学方程式为 ,反应中的还原剂为 ;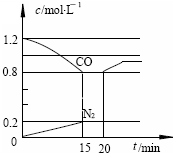
(3)D气体和CO都是汽车尾气的主要成分,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2D(g)+2CO(g)?N2(g)+2CO2(g);△H<0.若在一定温度下,将1.4mol D、1.2mol CO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.
①该反应的化学平衡常数为 K= ;
②若保持温度不变,20min 时再向容器中充入CO、N2各0.8mol,平衡将 移动(填“向左”、“向右”或“不”)
③20min时,若改变反应条件,导致CO浓度发生如图所示的变化,则改变的条件可能是 (填序号);
a.缩小容器体积 b.增加CO2 的量 c.升高温度 d.加入催化剂.
查看习题详情和答案>>
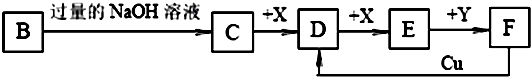
请回答下列问题:
(1)B的化学式为
(2)C可与过量的Cl2 反应生成HCl和物质A,A可发生水解反应生成NH3和HClO,则C与过量Cl2反应的化学方程式为

(3)D气体和CO都是汽车尾气的主要成分,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2D(g)+2CO(g)?N2(g)+2CO2(g);△H<0.若在一定温度下,将1.4mol D、1.2mol CO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.
①该反应的化学平衡常数为 K=
②若保持温度不变,20min 时再向容器中充入CO、N2各0.8mol,平衡将
③20min时,若改变反应条件,导致CO浓度发生如图所示的变化,则改变的条件可能是
a.缩小容器体积 b.增加CO2 的量 c.升高温度 d.加入催化剂.
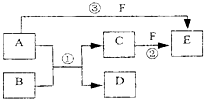 A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应,B、C、F都是气态单质,且B为黄绿色;反应③中有水生成,反应②需要放电才能发生,A和 D相遇有白烟生成.
(1)反应③的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
(2)反应①中每生成1mol C,转移的电子数为
3.612×1024
3.612×1024
;(3)A与D的水溶液恰好完全反应时,其生成物的水溶液呈
酸
酸
性(填“酸”“碱”或“中”),该水溶液中存在着如下关系,用粒子浓度符号填写:①c(H+)+
c(NH4+)
c(NH4+)
=c(OH-)+c(Cl-)
c(Cl-)
;②c(H+)=c(OH-)+
c(NH3?H2O)
c(NH3?H2O)
.(4)元素x与组成B的元素同周期,x的单质既可与酸反应也可与碱反应且都生成H2,则
①X的单质与碱反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;②X、空气、海水可以组成新型海水标志灯的电池.该种灯以海水为电解质溶液,靠空气中的氧气使X不断氧化而源源不断产生电流,只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20~50倍.则该新型电池的正极的电极反应式为
O2+H2O+4e-=4OH-
O2+H2O+4e-=4OH-
;原电池的总反应方程式为4Al+3O2+6H2O=4Al(OH)3
4Al+3O2+6H2O=4Al(OH)3
.