摘要:24. 答: 答:
网址:http://m.1010jiajiao.com/timu3_id_267418[举报]
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:
M2++2OH- M(OH)2
M(OH)2  2H++MO22-
2H++MO22-
回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25C° 时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-)
(2)25C° 时,向A的稀溶液中加入少量的烧碱固体.则水的电离度
Ⅱ、.室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为
查看习题详情和答案>>
M2++2OH-
 M(OH)2
M(OH)2  2H++MO22-
2H++MO22-回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25C° 时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-)
不变
不变
,C(H+)不变
不变
,水的电离度不变
不变
,Kw不变
不变
(2)25C° 时,向A的稀溶液中加入少量的烧碱固体.则水的电离度
减小
减小
,溶液的pH增大
增大
Ⅱ、.室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为
小于
小于
10 (填大于、等于或小于)Ⅰ、醉驾对人们的安全危害很大,利用下列原理可以检查司机是否酒后开车.
2K2Cr2O7(橙色)+3C2H5OH+H2SO4→Cr2(SO4)3(绿色)+K2SO4+CH3COOH+H2O
①配平化学方程式后,H2O前面的系数为
②怎样判断司机是酒后开车:
③写出用粮食酿酒的化学方程式:
Ⅱ、下列框图中,A由两种黑色金属氧化物等物质的量混合而成,B中含有四种阳离子.据此回答下列问题:

(1)A的组成是
(2)相同条件下,溶液B中所有阳离子的氧化性由强到弱的顺序依次是
(3)A中某组分可由单质与水反应制得,化学方程式为:
(4)电解所用装置如图所示.
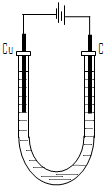
①电解开始阶段,阳极上的电极反应是
阴极上的电极反应是
②电解至阴极刚开始有固体R析出时,该溶液中金属离子浓度由大到小
的顺序是
查看习题详情和答案>>
2K2Cr2O7(橙色)+3C2H5OH+H2SO4→Cr2(SO4)3(绿色)+K2SO4+CH3COOH+H2O
①配平化学方程式后,H2O前面的系数为
11
11
;②怎样判断司机是酒后开车:
将司机呼出的气体通入橙色溶液中,观察溶液颜色是否向绿色转变
将司机呼出的气体通入橙色溶液中,观察溶液颜色是否向绿色转变
.③写出用粮食酿酒的化学方程式:
(C6H10O5)n+nH2O
nC6H12O6,C6H12O6
2C2H5OH+2CO2↑
| ||
| ||
| 酵母菌 |
(C6H10O5)n+nH2O
nC6H12O6,C6H12O6
2C2H5OH+2CO2↑
.
| ||
| ||
| 酵母菌 |
Ⅱ、下列框图中,A由两种黑色金属氧化物等物质的量混合而成,B中含有四种阳离子.据此回答下列问题:

(1)A的组成是
Fe3O4、CuO
Fe3O4、CuO
(填化学式).(2)相同条件下,溶液B中所有阳离子的氧化性由强到弱的顺序依次是
Fe3+>Cu2+>H+>Fe2+(全对给分)
Fe3+>Cu2+>H+>Fe2+(全对给分)
.(3)A中某组分可由单质与水反应制得,化学方程式为:
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.
| ||
(4)电解所用装置如图所示.

①电解开始阶段,阳极上的电极反应是
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
,阴极上的电极反应是
2 Fe3++2e-=2 Fe2+
2 Fe3++2e-=2 Fe2+
.②电解至阴极刚开始有固体R析出时,该溶液中金属离子浓度由大到小
的顺序是
Fe2+>Cu2+
Fe2+>Cu2+
.Ⅰ、在一定温度下,氧化铁可以与一氧化碳发生反应:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g).已知该反应在不同温度下的平衡常数如下表:
请回答下列问题:
该反应的平衡常数表达式K=
Ⅱ、工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
(1)容器①中反应达平衡时,CO的转化率为
(2)计算容器②中反应的平衡常数K=
(3)下列叙述正确的是
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q>65.6kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,化学反应速率为:v(H2O)=
mol/(L?min)
查看习题详情和答案>>
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g).已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
该反应的平衡常数表达式K=
K=
| c3(CO3) |
| c3(CO) |
K=
,△H| c3(CO3) |
| c3(CO) |
<
<
0(填“>”、“<”或“=”).Ⅱ、工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
80%
80%
.(2)计算容器②中反应的平衡常数K=
1
1
.(3)下列叙述正确的是
a
a
(填字母序号).a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q>65.6kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,化学反应速率为:v(H2O)=
| 4 |
| Vt1 |
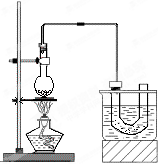 、实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)
、实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL80%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应.
回答下列问题:
(1)该实验制取溴乙烷的化学方程式为:
NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O
| △ |
NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O
| △ |
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为
Br2
Br2
,同时还生成另一种无色气体.(3)U型管内可观察到的现象是
有油状液体生成
有油状液体生成
.(4)反应结束后,U形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的
C
C
(填字母)A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
所需的主要玻璃仪器是
分液漏斗
分液漏斗
(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行蒸馏
蒸馏
(填操作名称).(5)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后
④①⑤③②
④①⑤③②
(填代号).①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(6)溴乙烷(C2H5Br)多一个碳的同系物所有可能的物质在氢氧化钠的醇溶液中能发生反应,写出该反应的化学方程式
CH3CH2CH2Br+NaOH
CH3CH=CH2+NaBr+H2O
| 醇 |
| △ |
CH3CH2CH2Br+NaOH
CH3CH=CH2+NaBr+H2O
,| 醇 |
| △ |
CH3CHBrCH3+NaOH
CH3CH=CH2+NaBr+H2O
| 醇 |
| △ |
CH3CHBrCH3+NaOH
CH3CH=CH2+NaBr+H2O
.| 醇 |
| △ |
 Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时向U型管两边各滴入几滴酚酞试液,试判断
①a是
正
正
极(填“正”或“负”);②B电极上的电极反应式为
2H++2e-═H2↑
2H++2e-═H2↑
,(2)如要用电解方法精炼粗铜,电解液c选用CuSO4溶液,则B电极的材料是
纯铜
纯铜
,电极反应式为Cu2++2e-═Cu
Cu2++2e-═Cu
.(3)用惰性电极电解CuSO4溶液.若阴极上析出Cu的质量为3.2g,则阳极上产生的气体在标准状况下的体积为
0.56L
0.56L
;Ⅱ、设计出燃料电池使汽油氧化直接产生电流是对21世纪最富有挑战性的课题之一.最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子.回答如下问题:
(1)以庚烷(C7H16)代表汽油,这个电池放电时发生的化学反应的化学方程式是:
C7H16+11O2=7CO2+8H2O
C7H16+11O2=7CO2+8H2O
(2)这个电池的负极发生的反应是:
C7H16+22O2--44e-=7CO2+8H2O
C7H16+22O2--44e-=7CO2+8H2O
;正极发生的反应是:11O2+44e-=22O2-
11O2+44e-=22O2-
;固体电解质里的O2-向负
负
(填“正”或“负”)极移动(1分)