摘要: 某有机物与氧气反应的产物是CH3CH2CHO, 原有机物是 A. 乙醇的同系物 B. 乙醛的同系物 C. 丙醇的同分异构体 D. 丙醛的同分异构体
网址:http://m.1010jiajiao.com/timu3_id_261628[举报]
 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.(1)写出硫铁矿与氧气反应的化学方程式:
4FeS2+11O2
2Fe2O3+8SO2
| ||
4FeS2+11O2
2Fe2O3+8SO2
| ||
工业上,该反应在
沸腾炉
沸腾炉
(填设备名称)中进行.(2)某含有SiO2的硫铁矿试样1克,在氧气中充分灼烧后残余固体为0.76g,则该硫铁矿式样的纯度为
72
72
%.已知SO3熔点16.83℃、沸点44.8℃.某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体.装置如图所示.(3)写出B中催化剂V2O5表面所发生的反应的化学方程式:
2SO2+O2
2SO3
| V2O5 |
| △ |
2SO2+O2
2SO3
.| V2O5 |
| △ |
(4)学生实验时发现在C装置U形管的右边有白雾生成.改进的办法是
CD之间连接一个装有浓硫酸的洗气瓶
CD之间连接一个装有浓硫酸的洗气瓶
.(5)装置D的作用是吸收尾气,其中干燥管的作用是
防止倒吸
防止倒吸
.装置D中所装液体试剂可能为D
D
.A.饱和食盐水
B.酒精
C.BaCl2溶液
D.NaOH溶液.
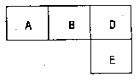 有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:(1)在B、D、E三种元素的最简单氢化物中,最稳定的是
H2O
H2O
(填化学式).M、D、E、N形成的简单离子的半径由大到小的关系是(用离子符号表示)S2->O2->Na+>H+
S2->O2->Na+>H+
.(2)A、B、D、M可组成多种18电子分子,请写出2种具有18电子的有机物的结构简式(用结构简式表示)
CH3OH
CH3OH
、CH3CH3
CH3CH3
.(3)由A、D、N三种元素组成的无机物(相对分子质量106),其水溶液呈碱性,用离子方程式表示其原因
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
.(4)元素B的氢化物与元素D单质一定条件下发生置换反应,在该反应中氧化剂与还原剂的物质的量之比为
3:4
3:4
.(5)在火箭推进器中装有强还原剂B2M4和强氧化剂M2D2,已知0.5mol液态B2M4和足量液态M2D2反应,生成一种无色无味无毒的气体和一种蒸气,放出320.8kJ热量,
H2O(1)=H2O(g)△H=+44kJ?mol-1
2M2D2(1)=2M2D(1)+D2(g)△H=-196.4kJ?mol-1
写出B2M4与氧气反应的热化学方程式为
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1;
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1;
.请写出B2M4、D2与KOH溶液组成的碱性电池的负极反应式(已知:B2M4可以和 D2反应生成B2和M2D)
N2H4-4e─+4OH─=N2+4H2O
N2H4-4e─+4OH─=N2+4H2O
;该电池中OH-移向负
负
极. 某课外活动小组做了如下关于钾的探究实验.
某课外活动小组做了如下关于钾的探究实验.(1)钾与水反应
实验中钾常会着火燃烧,并发生轻微爆炸,由此现象可以得出的结论是
钾与水反应放热
钾与水反应放热
(任写一个),该反应的离子方程式是2K++2H2O=2K++2OH-+H2↑
2K++2H2O=2K++2OH-+H2↑
.(2)钾与氯气反应
该实验中可选用如下方案制备氯气,其中最合理的是
B
B
(填序号).| 方案序号 | 所用试剂 | 净化剂 | 干燥剂 |
| A | MnO2、稀盐酸 | 饱和食盐水 | 浓硫酸 |
| B | Ca(ClO)2、浓盐酸 | 饱和食盐水 | 无水硫酸铜 |
| C | 氯酸钾、浓盐酸 | 饱和碳酸钠溶液 | 浓硫酸 |
| D | KMnO4、浓盐酸 | 水 | 碱石灰 |
D
D
(填序号).A.长颈漏斗 B.圆底烧瓶
C.酒精灯 D.洗气瓶
(3)钾与氧气反应的实验
经查找资料知:钾与氧气反应可能生成K2O、K2O2、KO2.
①取一定量的钾在空气中点燃,使其充分反应;
②将生成物研成细粉备用;
③常温下,利用如图所示装置探究生成物成分及含量.
据此回答下列问题:
①使细粉末与水反应的操作是
将仪器A向左倾斜,使水与样品充分接触
将仪器A向左倾斜,使水与样品充分接触
.②测量气体体积时应注意的事项是
将气体冷却到室温,移动量筒使量筒内外液面相平,使量筒内的气体压强与大气压相等,平视读数
将气体冷却到室温,移动量筒使量筒内外液面相平,使量筒内的气体压强与大气压相等,平视读数
.③若钾与氧气燃烧的产物为K2O2、KO2,取燃烧产物3.94g进行上述实验,测得气体的体积为868.0mL,则KO2的质量分数约为
72.08%
72.08%
.(已知:常温下,气体的摩尔体积为24.8L/mol)
(2011?浙江)食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.已知:氧化性:IO3->Fe3+>I2;还原性:S2O32->I-3I2+6OH-═IO3-+5I-+3H2O;
KI+I2 KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①加KSCN溶液显红色,该红色物质是
 (用电子式表示).
(用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境下KI与氧气反应的化学方程式:
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是
A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+.
查看习题详情和答案>>
KI+I2
 KI3
KI3(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①加KSCN溶液显红色,该红色物质是
Fe(SCN)3
Fe(SCN)3
(用化学式表示);CCl4中显紫红色的物质是

②第二份试液中加入足量KI固体后,反应的离子方程式为
IO3-+5I-+6H+═3I2+3H2O
IO3-+5I-+6H+═3I2+3H2O
、2Fe3++2I-═2Fe2++I2
2Fe3++2I-═2Fe2++I2
.(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境下KI与氧气反应的化学方程式:
4KI+O2+2H2O═2I2+4KOH
4KI+O2+2H2O═2I2+4KOH
.将I2溶于KI溶液,在低温条件下,可制得KI3?H2O.该物质作为食盐加碘剂是否合适?否
否
(填“是”或“否”),并说明理由KI3受热(或潮湿)条件下产生KI和I2,KI被氧气氧化,I2易升华
KI3受热(或潮湿)条件下产生KI和I2,KI被氧气氧化,I2易升华
.(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是
AC
AC
.A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+.
取足量该加碘盐溶于蒸馏水中,用盐酸酸化,滴加适量氧化剂(如:氯水、过氧化氢等),再滴加KSCN溶液,若显血红色,则该加碘盐中存在Fe2+
取足量该加碘盐溶于蒸馏水中,用盐酸酸化,滴加适量氧化剂(如:氯水、过氧化氢等),再滴加KSCN溶液,若显血红色,则该加碘盐中存在Fe2+
.(2013?莱芜一模)食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.
已知:①氧化性:
>Fe3+>I2;还原性:
>I-;②KI+I2?KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为4份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.向第二份试液中加入足量KI固体后,反应的离子方程式为:
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:
(3)某同学为探究温度和反应物浓度对反应2IO3-+5SO32-+2H+═I2+5SO42-+H2O的速率的影响,设计实验如下表所示:
表中数据:t1
查看习题详情和答案>>
已知:①氧化性:
| IO | - 3 |
| S2O | 2- 3 |
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为4份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.向第二份试液中加入足量KI固体后,反应的离子方程式为:
IO3-+5I-+6H+=3I2+3H2O
IO3-+5I-+6H+=3I2+3H2O
、2Fe3++2I-=2Fe2++I2
2Fe3++2I-=2Fe2++I2
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:
O2+4I-+2H2O=2I2+4KOH
O2+4I-+2H2O=2I2+4KOH
.(3)某同学为探究温度和反应物浓度对反应2IO3-+5SO32-+2H+═I2+5SO42-+H2O的速率的影响,设计实验如下表所示:
| 0.01mol?L-1KIO3 酸性溶液(含淀粉) 的体积/mL |
0.01mol?L-Na2SO3 溶液的体积/mL |
H2O的 体积/mL |
实验 温度 /℃ |
溶液出现 蓝色时所 需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | t1 |
| 实验2 | 5 | 5 | 40 | 25 | t2 |
| 实验3 | 5 | 5 | V2 | 0 | t3 |
<
<
t2(填“>”、“<”或“=”);表中V2=40
40
mL.