题目内容
 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.(1)写出硫铁矿与氧气反应的化学方程式:
4FeS2+11O2
2Fe2O3+8SO2
| ||
4FeS2+11O2
2Fe2O3+8SO2
| ||
工业上,该反应在
沸腾炉
沸腾炉
(填设备名称)中进行.(2)某含有SiO2的硫铁矿试样1克,在氧气中充分灼烧后残余固体为0.76g,则该硫铁矿式样的纯度为
72
72
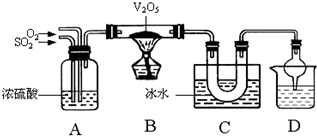
%.已知SO3熔点16.83℃、沸点44.8℃.某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体.装置如图所示.(3)写出B中催化剂V2O5表面所发生的反应的化学方程式:
2SO2+O2
2SO3
| V2O5 |
| △ |
2SO2+O2
2SO3
.| V2O5 |
| △ |
(4)学生实验时发现在C装置U形管的右边有白雾生成.改进的办法是
CD之间连接一个装有浓硫酸的洗气瓶
CD之间连接一个装有浓硫酸的洗气瓶
.(5)装置D的作用是吸收尾气,其中干燥管的作用是
防止倒吸
防止倒吸
.装置D中所装液体试剂可能为D
D
.A.饱和食盐水
B.酒精
C.BaCl2溶液
D.NaOH溶液.
分析:(1)硫铁矿和氧气反应生成氧化铁和二氧化硫气体,固体在沸腾炉中反应;
(2)依据化学方程式的差量变化计算硫化亚铁的纯度;
(3)根据SO2和O2在催化剂V2O5的作用下制备SO3固体写出反应的化学方程式;
(4)CD间加一个除去水蒸气的装置;
(5)装置D的作用是吸收尾气,其中干燥管的作用是防止倒吸,装置D中是吸收过量二氧化硫气体;
(2)依据化学方程式的差量变化计算硫化亚铁的纯度;
(3)根据SO2和O2在催化剂V2O5的作用下制备SO3固体写出反应的化学方程式;
(4)CD间加一个除去水蒸气的装置;
(5)装置D的作用是吸收尾气,其中干燥管的作用是防止倒吸,装置D中是吸收过量二氧化硫气体;
解答:解:(1)硫铁矿和氧气反应生成氧化铁和二氧化硫气体,反应的化学方程式为:4FeS2+11O2
2Fe2O3+8SO2 固体在沸腾炉中反应;
故答案为:4FeS2+11O2
2Fe2O3+8SO2、沸腾炉;
(2)设硫化亚铁质量为x
4FeS2+11O2
2Fe2O3+8SO2△m
480 160
x 1-0.76
x=0.72g
该硫铁矿式样的纯度=
×100%=72%
故答案为:72%;
(3)B中催化剂V2O5表面所发生的反应的化学方程式2SO2+O2
2SO3;
故答案为:2SO2+O2
2SO3;
(4)C装置U形管的右边有白雾生成,因为含有水蒸气,需要加入吸收水蒸气的装置,CD之间连接一个装有浓硫酸的洗气瓶;
故答案为:CD之间连接一个装有浓硫酸的洗气瓶;
(5)装置D的作用是吸收尾气,其中干燥管的作用是防止倒吸,D中液体是吸收二氧化硫气体的作用;
故答案为:防止倒吸、D;
| ||
故答案为:4FeS2+11O2
| ||
(2)设硫化亚铁质量为x
4FeS2+11O2
| ||
480 160
x 1-0.76
x=0.72g
该硫铁矿式样的纯度=
| 0.72g |
| 1g |
故答案为:72%;
(3)B中催化剂V2O5表面所发生的反应的化学方程式2SO2+O2
| V2O5 |
| △ |
故答案为:2SO2+O2
| V2O5 |
| △ |
(4)C装置U形管的右边有白雾生成,因为含有水蒸气,需要加入吸收水蒸气的装置,CD之间连接一个装有浓硫酸的洗气瓶;
故答案为:CD之间连接一个装有浓硫酸的洗气瓶;
(5)装置D的作用是吸收尾气,其中干燥管的作用是防止倒吸,D中液体是吸收二氧化硫气体的作用;
故答案为:防止倒吸、D;
点评:本题考查了工业制硫酸的原理方向判断,装置选择和原理应用,题目难度中等.

练习册系列答案
相关题目
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法。
(1)写出硫铁矿与氧气反应的化学方程式:
工业上,该反应在 (填设备名称)中进行。
(2)某含有SiO2的硫铁矿试样1克,在氧气中充分灼烧后残余固体为0.76g,则该硫铁矿式样的纯度为 %
已知SO3熔点16.83℃、沸点44.8℃。某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体。装置如下图所示
 |
(3)写出B中催化剂V2O5表面所发生的反应的化学方程式:
(4)学生实验时发现在C装置U形管的右边有白雾生成。改进的办法是 。
(5)装置D的作用是吸收尾气,其中干燥管的作用是 。装置D
中所装液体试剂可能为( )
A.饱和食盐水 B.酒精 C.BaCl2溶液 D.NaOH溶液
 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.