��Ŀ����
 ij����С���������¹��ڼص�̽��ʵ�飮
ij����С���������¹��ڼص�̽��ʵ�飮��1������ˮ��Ӧ
ʵ���мس����Ż�ȼ�գ�����������ը���ɴ�������Եó��Ľ�����
����ˮ��Ӧ����
����ˮ��Ӧ����
����дһ�������÷�Ӧ�����ӷ���ʽ��2K++2H2O=2K++2OH-+H2��
2K++2H2O=2K++2OH-+H2��
����2������������Ӧ
��ʵ���п�ѡ�����·����Ʊ��������������������
B
B
������ţ���| ������� | �����Լ� | ������ | ����� |
| A | MnO2��ϡ���� | ����ʳ��ˮ | Ũ���� |
| B | Ca��ClO��2��Ũ���� | ����ʳ��ˮ | ��ˮ����ͭ |
| C | ����ء�Ũ���� | ����̼������Һ | Ũ���� |
| D | KMnO4��Ũ���� | ˮ | ��ʯ�� |
D
D
������ţ���A������©�� B��Բ����ƿ
C���ƾ��� D��ϴ��ƿ
��3������������Ӧ��ʵ��
����������֪������������Ӧ��������K2O��K2O2��KO2��
��ȡһ�����ļ��ڿ����е�ȼ��ʹ���ַ�Ӧ��
�ڽ��������г�ϸ�۱��ã�
�۳����£�������ͼ��ʾװ��̽��������ɷּ�������
�ݴ˻ش��������⣺
��ʹϸ��ĩ��ˮ��Ӧ�IJ�����
������A������б��ʹˮ����Ʒ��ֽӴ�
������A������б��ʹˮ����Ʒ��ֽӴ�
���ڲ����������ʱӦע���������
��������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ���
��������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ���
��������������ȼ�յIJ���ΪK2O2��KO2��ȡȼ�ղ���3.94g��������ʵ�飬�����������Ϊ868.0mL����KO2����������ԼΪ
72.08%
72.08%
������֪�������£������Ħ�����Ϊ24.8L/mol��
��������1���غ�ˮ��Ӧ�Ƿ��ȷ�Ӧ����Ӧ�����������غ�������
��2������ԭ�Ϻͷ�Ӧ������ѡ����Ʊ������ķ�Ӧԭ�������жϣ�
��3���ٷ�ĩ��ˮ�Ӵ�������Ӧ��
��������ȴ������ѹǿ��ͬʱ����Һ����ƽ��ƽ�Ӷ�����
�����ݻ�ѧ����ʽ��ʽ���㣻
��2������ԭ�Ϻͷ�Ӧ������ѡ����Ʊ������ķ�Ӧԭ�������жϣ�
��3���ٷ�ĩ��ˮ�Ӵ�������Ӧ��
��������ȴ������ѹǿ��ͬʱ����Һ����ƽ��ƽ�Ӷ�����
�����ݻ�ѧ����ʽ��ʽ���㣻
����⣺��1���غ�ˮ������Ӧ�����Ż�ȼ�գ�����������ը��˵����Ӧ�Ƿ��ȷ�Ӧ����Ӧ�����ӷ���ʽΪ��2K++2H2O=2K++2OH-+H2����
�ʴ�Ϊ������ˮ��Ӧ���ȣ�2K++2H2O=2K++2OH-+H2����
��2��A��MnO2��ϡ����ܷ�Ӧ������������A����
B��Ca��ClO��2����ǿ������������Ũ��������������ͨ������ʳ��ˮ��ȥ�Ȼ��⣬ͨ����ˮ����ͭ����ˮ��������B��ȷ��
C������ء�Ũ���ᷴӦ����������ͨ�뱥��̼������Һ�����Ȼ��ⷴӦ���ɶ�����̼��Ҳ����������Ӧ����C����
D��KMnO4����ǿ����������Ũ��������������ˮ��ȥ�Ȼ��⣬ͬʱ������������ʯ�һ�������������D����
��ѡB��
�Ʊ�������ľ���װ����Ҫ��ϴ��ƿ���У�����Һ���÷�Һ©������Ӧ�����������Թܡ���ƿ�ȣ���Ӧ�е���Ҫ���ȷ�Ӧ���еij��·�Ӧ����ѡD��
��3����ʹϸ��ĩ��ˮ��Ӧ�IJ�����������A������б��ʹˮ����Ʒ��ֽӴ�������Ӧ��
�ʴ�Ϊ��������A������б��ʹˮ����Ʒ��ֽӴ���
������ʵ��װ�ã������������ʱӦע��������ǣ���������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ�����
�ʴ�Ϊ����������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ�����
������Ʒ��K2O2Ϊ xmol��KO2���ʵ���Ϊymol�����ݻ�ѧ����ʽ2K2O2+2H2O=4NaOH+O����4KO2+2H2O=4KOH+3O2����
�õ�110x+71y=3.94
+
=
��ã�x=0.01��y=0.04��
����KO2����������=
��100%=72.08%
�ʴ�Ϊ��72.08%
�ʴ�Ϊ������ˮ��Ӧ���ȣ�2K++2H2O=2K++2OH-+H2����
��2��A��MnO2��ϡ����ܷ�Ӧ������������A����
B��Ca��ClO��2����ǿ������������Ũ��������������ͨ������ʳ��ˮ��ȥ�Ȼ��⣬ͨ����ˮ����ͭ����ˮ��������B��ȷ��
C������ء�Ũ���ᷴӦ����������ͨ�뱥��̼������Һ�����Ȼ��ⷴӦ���ɶ�����̼��Ҳ����������Ӧ����C����
D��KMnO4����ǿ����������Ũ��������������ˮ��ȥ�Ȼ��⣬ͬʱ������������ʯ�һ�������������D����
��ѡB��
�Ʊ�������ľ���װ����Ҫ��ϴ��ƿ���У�����Һ���÷�Һ©������Ӧ�����������Թܡ���ƿ�ȣ���Ӧ�е���Ҫ���ȷ�Ӧ���еij��·�Ӧ����ѡD��
��3����ʹϸ��ĩ��ˮ��Ӧ�IJ�����������A������б��ʹˮ����Ʒ��ֽӴ�������Ӧ��
�ʴ�Ϊ��������A������б��ʹˮ����Ʒ��ֽӴ���
������ʵ��װ�ã������������ʱӦע��������ǣ���������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ�����
�ʴ�Ϊ����������ȴ�����£��ƶ���Ͳʹ��Ͳ����Һ����ƽ��ʹ��Ͳ�ڵ�����ѹǿ�����ѹ��ȣ�ƽ�Ӷ�����
������Ʒ��K2O2Ϊ xmol��KO2���ʵ���Ϊymol�����ݻ�ѧ����ʽ2K2O2+2H2O=4NaOH+O����4KO2+2H2O=4KOH+3O2����
�õ�110x+71y=3.94
| x |
| 2 |
| 3y |
| 4 |
| 0.868 |
| 24.8 |
��ã�x=0.01��y=0.04��
����KO2����������=
| 0.04��71 |
| 3.94 |
�ʴ�Ϊ��72.08%
���������⿼���������ʵ�Ӧ�ã�����ʵ�����Ʊ����������徻���Լ�ѡ��ѧ����ʽ���㣬ʵ��������������գ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
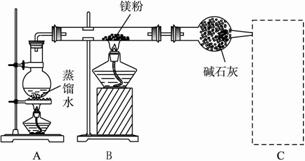
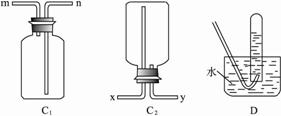
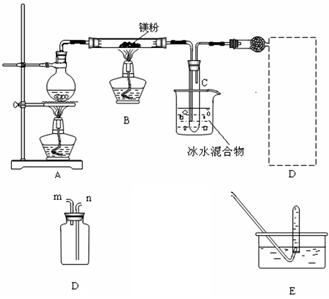
 �ȹ۲쵽���������ٵ�ȼ��һ�ƾ��ơ���������Ŀ������������������
�ȹ۲쵽���������ٵ�ȼ��һ�ƾ��ơ���������Ŀ������������������ Ӧһ��ʱ���Bװ�ò������п��ܲ����Ĺ������ʳ�MgO�⣬������M
Ӧһ��ʱ���Bװ�ò������п��ܲ����Ĺ������ʳ�MgO�⣬������M g��Mg(OH)2 ��ѡ����һ�֣����ʵ��֤�����Ĵ��ڣ���Ҫд����Ҫ�����������Լ��������ۡ�
g��Mg(OH)2 ��ѡ����һ�֣����ʵ��֤�����Ĵ��ڣ���Ҫд����Ҫ�����������Լ��������ۡ�