摘要:填表 溶液名称 氢氧化钠 稀硫酸 澄清石灰水 碘酒 盐酸 酒精的水溶液 溶质名称 溶剂名称
网址:http://m.1010jiajiao.com/timu3_id_25711[举报]
(2011?日照)下列装置用于实验室里CO2的制备、净化、检验,最后收集一瓶干燥的CO2.请回答下列问题:

(1)对实验室制取二氧化碳药品选择的探究实验,记录如下:
从制取和收集的角度分析,一般选择第
(2)把C、D中的液体名称填入下表:
(3)B中反应的化学方程式是
(4)C中反应的化学方程式是
(5)反应过程中将弹簧夹关闭,在A中看到的现象是
(6)E收集方法说明二氧化碳具有的物理性质是
查看习题详情和答案>>

(1)对实验室制取二氧化碳药品选择的探究实验,记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
③
③
(填序号)组药品,所发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.(2)把C、D中的液体名称填入下表:
| B(盐) | C(碱) | D(酸) | |
| 液体名称 | 碳酸氢钠溶液 | 澄清石灰水 澄清石灰水 | 浓硫酸 浓硫酸 |
NaHCO3+HCl═NaCl+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
.(4)C中反应的化学方程式是
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.(5)反应过程中将弹簧夹关闭,在A中看到的现象是
A中锥形瓶内液面下降;长颈漏斗内液面上升
A中锥形瓶内液面下降;长颈漏斗内液面上升
.(6)E收集方法说明二氧化碳具有的物理性质是
二氧化碳的密度比空气大
二氧化碳的密度比空气大
.某活动小组分别用紫色牵牛花、大红色的月季花、紫萝卜花、丝瓜花提取指示剂.
(1)步骤1:用研钵将花分别捣烂.其目的是________.
(2)乙醇中其中起到的作用是( )
A.催化剂
B.参加化学反应
C.溶质
D.溶剂
步骤2:将步骤1得到的混合物,用纱布过滤.
(3)过滤的目的是________.
步骤3:将步骤2得到的滤液分别滴入到澄清石灰水和食醋中.得到的现象如下表所示:

(4)上述四种滤液,最不适合做酸碱指示剂的________(填植物名称).
(5)将月季花的滤液滴入稀盐酸中,溶液呈________色;滴入氢氧化钠的溶液中,溶液呈________色.
(6)将牵牛花的滤液滴入某溶液中呈黄绿色,则该溶液可能是( )
A.氢氧化钠溶液
B.稀硫酸
C.汽水
D.食盐水
(2013?镇江模拟)兴趣小组参观某制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
②反应原理:NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl,将分离出的晶体A充分加热,可制得纯碱.
③NH4Cl
NH3↑+HCl↑.
④无水硫酸铜遇水变蓝
⑤部分生产流程如下图所示: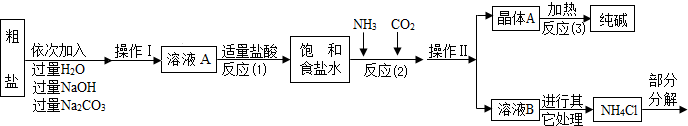
【问题讨论】
(1)①写出加入氢氧化钠溶液所发生反应的化学方程式
②操作Ⅱ的名称为
③反应(1)中加适量盐酸的作用是
④反应(2)中为提高产率,所加气体的顺序是
A.先通入二氧化碳再通氨气 B.先通入氨气再通二氧化碳
(2)上述生产流程中不可循环使用的是
A.CO2 B.NH3 C.HCl D.NaOH
【组成探究一】
(3)①晶体A受热分解的化学方程式为
②设计实验检验纯碱样品中是否混有晶体A请完成下表:

【组成探究二】
(4)取纯碱样品加水溶解,向其中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
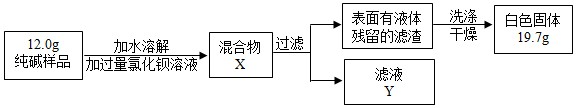
①判断加入BaCl2溶液是否过量的合适方法是
A.静置混合物X,向上层清液中再滴BaCl2溶液
B.向滤液Y中滴加BaCl2溶液
②判断滤渣是否洗涤干净,可采取向洗涤液中滴加
A.BaCl2溶液 B.稀H2SO4 C.Na2CO3溶液 D.稀HCl
③根据实验数据,计算样品中碳酸钠的质量分数为
查看习题详情和答案>>
【查阅资料】
①粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
②反应原理:NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl,将分离出的晶体A充分加热,可制得纯碱.
③NH4Cl
| ||
④无水硫酸铜遇水变蓝
⑤部分生产流程如下图所示:

【问题讨论】
(1)①写出加入氢氧化钠溶液所发生反应的化学方程式
2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
.②操作Ⅱ的名称为
过滤
过滤
.③反应(1)中加适量盐酸的作用是
除去过量的氢氧化钠和碳酸钠
除去过量的氢氧化钠和碳酸钠
.④反应(2)中为提高产率,所加气体的顺序是
B
B
(填字母).A.先通入二氧化碳再通氨气 B.先通入氨气再通二氧化碳
(2)上述生产流程中不可循环使用的是
D
D
(填字母).A.CO2 B.NH3 C.HCl D.NaOH
【组成探究一】
(3)①晶体A受热分解的化学方程式为
2NaHCO3
Na2CO3+H2O+CO2↑;
| ||
2NaHCO3
Na2CO3+H2O+CO2↑;
.
| ||
②设计实验检验纯碱样品中是否混有晶体A请完成下表:

| 选择的装置 | 实验现象 | 实验结论 |
AB AB |
B中澄清石灰水不变浑浊 B中澄清石灰水不变浑浊 |
样品不含晶体A |
(4)取纯碱样品加水溶解,向其中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为
AgNO3+NaCl═AgCl↓+NaNO3
AgNO3+NaCl═AgCl↓+NaNO3
,确定纯碱样品含有杂质NaCl.【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:

①判断加入BaCl2溶液是否过量的合适方法是
A
A
,观察现象判断.A.静置混合物X,向上层清液中再滴BaCl2溶液
B.向滤液Y中滴加BaCl2溶液
②判断滤渣是否洗涤干净,可采取向洗涤液中滴加
BC
BC
,观察现象判断.A.BaCl2溶液 B.稀H2SO4 C.Na2CO3溶液 D.稀HCl
③根据实验数据,计算样品中碳酸钠的质量分数为
88.3%
88.3%
(写出计算过程)某化学活动小组以“酸碱盐的性质”为主题,进行探究学习,请你作为该小组成员来解决下列问题.
(1)实验前,小组同学对某些问题展开讨论并设计有关实验方案:
①小刚同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”.你认为这种推理
(填“正确”或“不正确”),你的例证是 .
②小丽同学从某一欠收农田里取回一份土壤样品,请你用两种不同的方法帮小丽测出该土壤样品浸出液的酸碱性(只写出所用试剂的名称即可):① ;② .
如果检测的结果呈酸性,那么要改良此土壤,应该向农田里施加 .
③请你设计一个实验,能通过清晰可见的现象,除去氯化钙溶液中的少量稀盐酸.你的实验方案是(写出实验操作、现象和结论) .
(2)配制溶液:实验中需用50g15%CuSO4溶液.
试计算:需用CuSO4 g,水 mL.
实验步骤是:计算、 、 .
负责量取溶剂水的小刚为准确量取水量需向实验老师领取的化学仪器有 .
小红去药品柜找不到白色CuSO4粉末,只有蓝色CuSO4晶体(CuSO4?5H2O),她应称取药品 g,同时通知小刚取水 mL.
(3)在实验过程中,小组同学遇到几个具体问题,请你帮助解决:
①小红同学在探究完氢氧化钠的性质后,忘了将瓶塞盖上,使氢氧化钠溶液敞口放置了一段时间.为了检验这瓶溶液是否变质,你设计的实验方案是 .
②有两种混合气体A、B,可能分别含有氢气、一氧化碳和二氧化碳中的一种或几种,现将它们分别依次通过足量的下表所示物质,试完成下表:
(提示:氢气能与氧化铜反应生成铜和水,无水硫酸铜遇水由白色变成蓝色)
(4)鉴别溶液中的离子:某溶液中只含有Na2SO4、Na2CO3和NaCl三种物质.欲证明其中SO42-、CO32-、C1-确实存在,他们设计了如下实验,请你认真填写下面的实验报告.
查看习题详情和答案>>
(1)实验前,小组同学对某些问题展开讨论并设计有关实验方案:
①小刚同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”.你认为这种推理
②小丽同学从某一欠收农田里取回一份土壤样品,请你用两种不同的方法帮小丽测出该土壤样品浸出液的酸碱性(只写出所用试剂的名称即可):①
如果检测的结果呈酸性,那么要改良此土壤,应该向农田里施加
③请你设计一个实验,能通过清晰可见的现象,除去氯化钙溶液中的少量稀盐酸.你的实验方案是(写出实验操作、现象和结论)
(2)配制溶液:实验中需用50g15%CuSO4溶液.
试计算:需用CuSO4
实验步骤是:计算、
负责量取溶剂水的小刚为准确量取水量需向实验老师领取的化学仪器有
小红去药品柜找不到白色CuSO4粉末,只有蓝色CuSO4晶体(CuSO4?5H2O),她应称取药品
(3)在实验过程中,小组同学遇到几个具体问题,请你帮助解决:
①小红同学在探究完氢氧化钠的性质后,忘了将瓶塞盖上,使氢氧化钠溶液敞口放置了一段时间.为了检验这瓶溶液是否变质,你设计的实验方案是
②有两种混合气体A、B,可能分别含有氢气、一氧化碳和二氧化碳中的一种或几种,现将它们分别依次通过足量的下表所示物质,试完成下表:
| 混合气体 | 澄清的石灰水 | 浓硫酸 | 灼热的氧化铜 | 无水硫酸铜 | 澄清的石灰水 | 结 论 |
| A | 无现象 | 黑色变红色 | 白色变蓝色 | 变浑浊 | ||
| B | 黑色变红色 | CO2、H2 |
(4)鉴别溶液中的离子:某溶液中只含有Na2SO4、Na2CO3和NaCl三种物质.欲证明其中SO42-、CO32-、C1-确实存在,他们设计了如下实验,请你认真填写下面的实验报告.
| 实 验 步 骤 | 实验现象 | 结 论 |
| 1.向盛该溶液的试管中加入足量稀HNO3 | 有气泡产生 | 证明有CO32- |
| 2.继续向试管中加足量 |
有白色沉淀生成 | 证明有 |
| 3.过滤,向滤液中加适量 |
有白色沉淀生成 | 证明有 |