网址:http://m.1010jiajiao.com/timu3_id_255144[举报]
I.将由Na+、Ba2+、Cu2+、SO42-、Cl-组合形成的三种强电解质溶液,分别装入图1装置中的甲、乙、丙三个烧杯中进行电解,电极均为石墨电极.
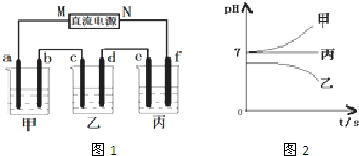
接通电源,经过一段时间后,测得乙中c电极质量增加.常温下各烧杯中溶液pH与电解时间t的关系如图2(忽略因气体溶解带来的影响).据此回答下列问题:
(1)写出乙烧杯中发生反应的化学方程式______;
(2)电极f上发生的电极反应为______;
(3)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是______.
II.工业上利用BaSO4制备BaCl2的工艺流程如下:
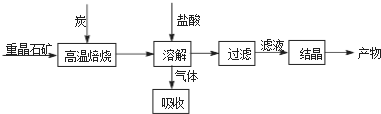
某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验.
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S.Na2S水溶液显碱性的原因是______(用离子方程式表示).
(2)已知有关反应的热化学方程式如下:
BaSO4(s)+4C(s)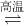 4CO(g)+BaS(s)△H1=+571.2kJ/mol
4CO(g)+BaS(s)△H1=+571.2kJ/mol
C(s)+CO2(g) 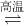 2CO(g)△H2=+172.5kJ/mol
2CO(g)△H2=+172.5kJ/mol
则反应BaSO4(s)+2C(s)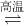 2CO2(g)+BaS(s)△H3=______kJ/mol
2CO2(g)+BaS(s)△H3=______kJ/mol
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是______,______.
查看习题详情和答案>>
Ⅰ.将由Na+、Ba2+、Cu2+、SO42-、Cl-组合形成的三种强电解质溶液,分别装入下图装置中的甲、乙、丙三个烧杯中进行电解,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液pH与电解时间t的关系如右上图(忽略因气体溶解带来的影响)。据此回答下列问题:

(1)在甲中烧杯中滴加酚酞, 极(填a或b)附近溶液会变红。
(2)写出乙烧杯中发生反应的化学方程式 。
(3)电极f上发生的电极反应式为 。
(4)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是 。
Ⅱ.工业上利用BaSO4制备BaCl2的工艺流程如下:
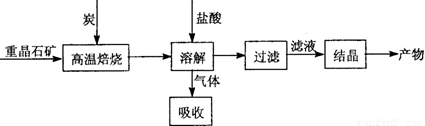
某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验。
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S。Na2S水溶液显碱性的原因是 。(用离子方程式表示)
(2)已知有关反应的热化学方程式如下:
BaSO4(s) +4C(s) 4CO(g)+BaS(s)
△H1 =
+571.2kJ/mol ①
4CO(g)+BaS(s)
△H1 =
+571.2kJ/mol ①
C(s) +CO2(g) 2CO(g)
△H2 =
+172.5kJ/mol
②
2CO(g)
△H2 =
+172.5kJ/mol
②
则反应BaSO4(s)
+2C(s) 2CO2(g)
+ BaS(s) △H3 =
2CO2(g)
+ BaS(s) △H3 =
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是 。
查看习题详情和答案>>
Ⅰ.将由Na+、Ba2+、Cu2+、SO42-、Cl-组合形成的三种强电解质溶液,分别装入下图装置中的甲、乙、丙三个烧杯中进行电解,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液pH与电解时间t的关系如右上图(忽略因气体溶解带来的影响)。据此回答下列问题: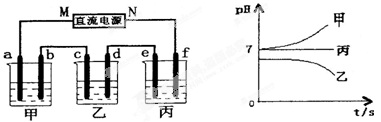
(1)在甲中烧杯中滴加酚酞, 极(填a或b)附近溶液会变红。
(2)写出乙烧杯中发生反应的化学方程式 。
(3)电极f上发生的电极反应式为 。
(4)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是 。
Ⅱ.工业上利用BaSO4制备BaCl2的工艺流程如下: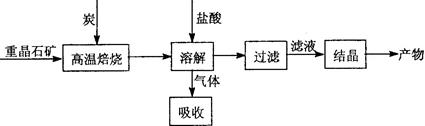
某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验。
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S。Na2S水溶液显碱性的原因是 。(用离子方程式表示)
(2)已知有关反应的热化学方程式如下:
BaSO4(s) +4C(s) 4CO(g)+BaS(s) △H1 = +571.2kJ/mol ①
4CO(g)+BaS(s) △H1 = +571.2kJ/mol ①
C(s) +CO2(g) 2CO(g) △H2 = +172.5kJ/mol ②
2CO(g) △H2 = +172.5kJ/mol ②
则反应BaSO4(s) +2C(s) 2CO2(g) + BaS(s) △H3 =
2CO2(g) + BaS(s) △H3 =
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是 。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液pH与电解时间t的关系如右上图(忽略因气体溶解带来的影响)。据此回答下列问题:

(1)在甲中烧杯中滴加酚酞, 极(填a或b)附近溶液会变红。
(2)写出乙烧杯中发生反应的化学方程式 。
(3)电极f上发生的电极反应式为 。
(4)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是 。
Ⅱ.工业上利用BaSO4制备BaCl2的工艺流程如下:

某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验。
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S。Na2S水溶液显碱性的原因是 。(用离子方程式表示)
(2)已知有关反应的热化学方程式如下:
BaSO4(s) +4C(s)
 4CO(g)+BaS(s) △H1 = +571.2kJ/mol ①
4CO(g)+BaS(s) △H1 = +571.2kJ/mol ①C(s) +CO2(g)
 2CO(g) △H2 = +172.5kJ/mol ②
2CO(g) △H2 = +172.5kJ/mol ②则反应BaSO4(s) +2C(s)
 2CO2(g) + BaS(s) △H3 =
2CO2(g) + BaS(s) △H3 = (3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是 。

接通电源,经过一段时间后,测得乙中c电极质量增加.常温下各烧杯中溶液pH与电解时间t的关系如图2(忽略因气体溶解带来的影响).据此回答下列问题:
(1)写出乙烧杯中发生反应的化学方程式
| ||
| ||
(2)电极f上发生的电极反应为
(3)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是
II.工业上利用BaSO4制备BaCl2的工艺流程如下:

某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验.
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S.Na2S水溶液显碱性的原因是
(2)已知有关反应的热化学方程式如下:
BaSO4(s)+4C(s)
| 高温 |
C(s)+CO2(g)
| 高温 |
则反应BaSO4(s)+2C(s)
| 高温 |
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是