摘要:19.氮有多种氧化物.其中之一的N2O3极不稳定.在液体或蒸气中大部分分离成NO和NO2.因而在NO氧化为NO2的过程中几乎没有N2O3生成.同样亚硝酸也不稳定.在微热甚至冷的条件下即分解.亚硝酸钠在中性或碱性条件中是稳定的.但酸化后能氧化KI.生成I2和NO气体.(1)亚硝酸分解的化学方程式是 (2)酸性溶液中亚硝酸钠和碘化钾反应制取NO的离子方程式是 .(3)在隔绝空气条件下.按下列操作制取NO:先取亚硝酸钠溶液适量加入稀盐酸片刻后.再加入KI溶液.试问这样的气体是否纯净? 为什么? .
网址:http://m.1010jiajiao.com/timu3_id_254597[举报]
氮有多种氧化物,其中N2O5是一种新型硝化剂,其性质和制备收到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)
 4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0
①反应达到平衡后,若再通入一定量氩气,则N2O5的转化率将___(填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
|
t/s |
0 |
500 |
1000 |
|
c(N2O5)/mol·L—1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为______________。
③一定温度下,在2L恒容密闭容器中加入2mol
N2O5,达到平衡时,气体的压强为原来的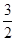 ,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的__________区生成,其电极反应式为_________________________________。

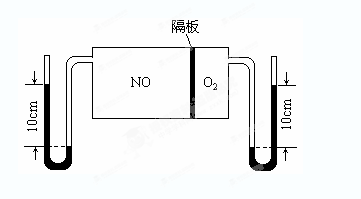
(3)如图:V(NO):V(O2)=3:1。当抽去NO和O2之间的隔板后,NO和O2反应后成NO2,部分NO2聚合成N2O4(N2O4此时为气态)。当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm。假设温度不变,且隔板及U形毛细管的体积都忽略不计,此时混合气体的平均相对分子质量为__________。
查看习题详情和答案>>
氮有多种氧化物,其中N2O3很不稳定,在液体或蒸汽中大部分都离解为NO和NO2,因而在NO转化为NO2的过程中几乎没有N2O3生成。亚硝酸也不稳定,在微热甚至冷的条件下也会分解。亚硝酸钠(NaNO2)在中性或碱性溶液中是稳定的,酸化后能氧化碘化钾生成单质碘和NO。
请填写下列空白:
(1)写出亚硝酸分解的化学方程式:___________________________________。
(2)写出在酸性溶液中用亚硝酸钠和碘化钾反应制取NO的离子方程式:______________________。
(3)在隔绝空气的条件下按以下操作制取NO:先取亚硝酸钠溶液适量,加入稀盐酸,片刻后,再加入碘化钾溶液,此时,所得气体是否纯净?___________,原因是_______________,应该怎样进行操作才能得到纯净的NO?__________________________________________________________________________。 查看习题详情和答案>>
请填写下列空白:
(1)写出亚硝酸分解的化学方程式:___________________________________。
(2)写出在酸性溶液中用亚硝酸钠和碘化钾反应制取NO的离子方程式:______________________。
(3)在隔绝空气的条件下按以下操作制取NO:先取亚硝酸钠溶液适量,加入稀盐酸,片刻后,再加入碘化钾溶液,此时,所得气体是否纯净?___________,原因是_______________,应该怎样进行操作才能得到纯净的NO?__________________________________________________________________________。 查看习题详情和答案>>
金属镁和镁合金在航空、汽车制造和电子工业等领域具有广泛的用途,金属镁的冶炼有多种方法,其中之一为皮江法.该方法是以白云石(CaCO3?MgCO3)为原料,经高温煅烧生成氧化物(CaO?MgO),氧化物在还原炉中经1200℃真空条件下用硅铁还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁.反应工艺流程如图1:
(1)在冶炼过程中反应温度对生成金属镁的影响如图2,从图中分析,还原反应的反应热△H 0(填“<”“>”“=”)理由是 .
(2)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
真空条件对制备金属镁来讲,可以达到的目的是:① ②
(3)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中KCl?MgCl2?6H2O属于 .
A.复盐 B.混合物 C.配合物
(4)写出煅烧白云石的反应化学方程式 .
查看习题详情和答案>>

(1)在冶炼过程中反应温度对生成金属镁的影响如图2,从图中分析,还原反应的反应热△H
(2)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
| 剩余压强mmHg | 760 | 10 | 1 | 0.1 |
| 平衡时的温度℃ | 2370 | 1700 | 1430 | 1235 |
(3)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中KCl?MgCl2?6H2O属于
A.复盐 B.混合物 C.配合物
(4)写出煅烧白云石的反应化学方程式
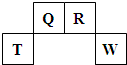 (2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
(2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.请回答下列问题:
(1)T的原子结构示意图为


(2)元素的非金属性为(原子的得电子能力):Q
弱于
弱于
W(填“强于”或“弱于”).(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
S+2H2SO4(浓)
3SO2↑+2H2O
.
| ||
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
NaNO2
NaNO2
.(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ.又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H=
(3a-4b)kJ?mol-1
(3a-4b)kJ?mol-1
(注:题中所涉单质均为最稳定单质). 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:(1)B、C、D元素电负性的大小顺序为:
O
O
>N
N
>C
C
(填元素符号).(2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为
8HCl+KClO4═KCl+4Cl2↑+4H2O
8HCl+KClO4═KCl+4Cl2↑+4H2O
.(3)C有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式
NaNO2
NaNO2
.(4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ.又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的△H=
-(4a-3b)KJ/mol
-(4a-3b)KJ/mol
(注:题中所设单质均为最稳定单质)(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成
将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成
(6)用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式
NO3-+3e-+4H+=NO↑+2H2O
NO3-+3e-+4H+=NO↑+2H2O
.(假设C只被还原至+2价)