摘要:将0.1mol/LK2CO3溶液中.由于CO的水解.使得c(CO)<0.1mol/L如果要使c(CO)更接近于0.1mol/L.可以采取的措施是 ( ) A.加入少量盐酸 B.加入适量的水 C.加入适当K2CO3 D.加热
网址:http://m.1010jiajiao.com/timu3_id_248020[举报]
在100℃时,将0.1mol的四氧化二氮气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
(1)该反应的化学方程式为
(2)20s时四氧化二氮的浓度C1=
查看习题详情和答案>>
| 浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4)/mol?L-1 | 0.1 | c1 | 0.05 | C3 | a | b |
| C(NO2)/mol?L-1 | 0 | 0.06 | C2 | 0.12 | 0.12 | 0.12 |
N2O4=2NO2
N2O4=2NO2
,达到平衡时四氧化二氮的转化率为60
60
%,表中C2>
>
C3=
=
a=
=
b(选填“>”、“<”、“═”).(2)20s时四氧化二氮的浓度C1=
0.07
0.07
mol?l-1,在0s~20s内四氧化二氮的平均反应速率为0.0015
0.0015
mol?(L?s)-1.(1)常温下,将0.1mol?L-1盐酸溶液和0.06mol?L-1氢氧化钡溶液等体积混合后,该混合溶液的pH=
(2)常温下,pH=a的10体积的某强酸与pH=b的1体积的某强碱混合后,溶液呈中性,则a和b满足的关系
(3)某温度时,水的离子积KW=1×10-13,则该温度
(4)常温下,pH=8的NH4Cl溶液中,c(Cl-)-c(NH4+)=
查看习题详情和答案>>
12
12
(混合后溶液体积的变化忽略不计)(2)常温下,pH=a的10体积的某强酸与pH=b的1体积的某强碱混合后,溶液呈中性,则a和b满足的关系
a+b=15
a+b=15
(混合后溶液体积的变化忽略不计)(3)某温度时,水的离子积KW=1×10-13,则该温度
>
>
25℃(选填“>”、“<”或“=”),若将此温度下pH=2的稀硫酸aL与pH=12的氢氧化钠溶液bL混合,若所得混合液的pH=11,则a:b=9:11
9:11
(混合后溶液体积的变化忽略不计)(4)常温下,pH=8的NH4Cl溶液中,c(Cl-)-c(NH4+)=
9.9×10-7mol/L
9.9×10-7mol/L
.(2010?西城区模拟)如图所示反应I、反应II和反应III均是工业生产中常见的反应.其中A、B为化合物,C是温室气体之一,D和K均可用做干燥剂,H常温下为液态化合物,J是一种具有漂白作用的盐,反应III和E与G反应的原理相同.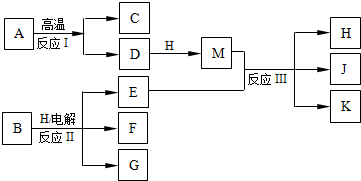
(1)C的电子式是
 .
.
(2)反应II的离子方程式是
(3)J久置后,即便不接触水、空气,本身也逐渐分解生成K,并放出气体,该反应的化学方程式是
(4)工业上测定反应III产品的有效成分J的含量,先将一定量的产品的溶液加入过量的KI溶液和稀硫酸中,使之反应生成I2,然后用Na2S2O3标准溶液滴定I2,计算出结果.
①用Na2S2O3标准溶液滴定I2时选用的指示剂是
②生成I2的反应的离子方程式是
(5)已知:2Fe2++Br2=2Fe3++2Br-.若将0.1mol E通入100mL FeBr2溶液中,溶液中有三分之一的Br-被氧化成Br2,则此反应离子方程式是
查看习题详情和答案>>

(1)C的电子式是


(2)反应II的离子方程式是
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
.
| ||
(3)J久置后,即便不接触水、空气,本身也逐渐分解生成K,并放出气体,该反应的化学方程式是
Ca(ClO)2═CaCl2+O2↑
Ca(ClO)2═CaCl2+O2↑
.(4)工业上测定反应III产品的有效成分J的含量,先将一定量的产品的溶液加入过量的KI溶液和稀硫酸中,使之反应生成I2,然后用Na2S2O3标准溶液滴定I2,计算出结果.
①用Na2S2O3标准溶液滴定I2时选用的指示剂是
淀粉
淀粉
.②生成I2的反应的离子方程式是
ClO-+2I-+2H+=Cl-+I2+H2O
ClO-+2I-+2H+=Cl-+I2+H2O
.(5)已知:2Fe2++Br2=2Fe3++2Br-.若将0.1mol E通入100mL FeBr2溶液中,溶液中有三分之一的Br-被氧化成Br2,则此反应离子方程式是
6Fe2++4Br-+5Cl25Cl2-═6Fe3++2Br2+10Cl-
6Fe2++4Br-+5Cl25Cl2-═6Fe3++2Br2+10Cl-
,原FeBr2溶液的物质的量浓度为1.2 mol/L
1.2 mol/L
.已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素.
(1)W在周期表中的位置: .
(2)在一定条件下,容积为1L密闭容器中加入1.2molX2和0.4molY2,发生如下反应:
3X2(g)+Y2(g)?2YX3(g)△H
反应各物质的量浓度随时间变化如图:
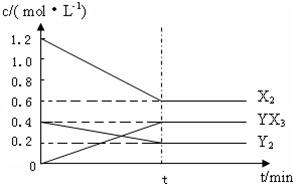
①此反应的平衡常数表达式为 (用化学式表示),K= .
②若升高温度平衡常数K减小,则△H 0(填“>”,“<”).
(3)A1是四种元素中三种元素组成的电解质,溶液呈碱性,将0.1mol?L-1的A1溶液稀释至原体积的10倍后溶液的pH=12,则A1的电子式为 .
(4)B1、B2是由四种元素三种形成的强电解质,且溶液呈酸性,相同浓度时B1溶液中水的电离程度小于B2溶液中水的电离程度,其原因是 .
(5)A2和B1反应生成B2,则0.2mol/LA2和0.1mol/L B1等体积混合后溶液中离子浓度大小关系为 .
查看习题详情和答案>>
(1)W在周期表中的位置:
(2)在一定条件下,容积为1L密闭容器中加入1.2molX2和0.4molY2,发生如下反应:
3X2(g)+Y2(g)?2YX3(g)△H
反应各物质的量浓度随时间变化如图:

①此反应的平衡常数表达式为
②若升高温度平衡常数K减小,则△H
(3)A1是四种元素中三种元素组成的电解质,溶液呈碱性,将0.1mol?L-1的A1溶液稀释至原体积的10倍后溶液的pH=12,则A1的电子式为
(4)B1、B2是由四种元素三种形成的强电解质,且溶液呈酸性,相同浓度时B1溶液中水的电离程度小于B2溶液中水的电离程度,其原因是
(5)A2和B1反应生成B2,则0.2mol/LA2和0.1mol/L B1等体积混合后溶液中离子浓度大小关系为