摘要:某混合气体12g.在标准状况下占体积5.6L.则该混合气体的平均相对分子质量是: ( ) A 24 B 48 C 36 D 72
网址:http://m.1010jiajiao.com/timu3_id_247267[举报]
(1)已知某混合气体的体积百分组成为80.0%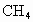 、15.0%
、15.0%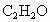 .请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
.请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
(2)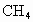 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成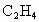 、
、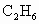 (水和其他产物忽略不计).取一定量
(水和其他产物忽略不计).取一定量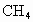 经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中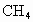 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中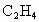 的体积百分含量.(本题计算过程中请保留3位有效数字)
的体积百分含量.(本题计算过程中请保留3位有效数字)
(1)已知某混合气体由体积分数为80%CH4、15%C2H4和5%CH2O组成。
请计算0.500mol该混合气体的质量和标准状况下的密度。
(2)CH4在一定条件下催化氧化可以生成C2H4、C2H6(水和其他反应产物忽略不计)。取一定量CH4催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g·L-1。已知反应中CH4消耗了20.0%,计算混合气体中C2H4的体积分数(本题计算过程中 请保留3位有效数字)。
查看习题详情和答案>>