网址:http://m.1010jiajiao.com/timu3_id_245506[举报]
 绿矾是一种重要的化工原料.
绿矾是一种重要的化工原料.【问题1】绿矾晶体(FeSO4?7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案.可供选择的试剂:KSCN溶液、酸性KMnO4溶液、氯水、NaOH溶液、BaCl2溶液请参与完成方案设计.
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
(1)方案1:取少量溶液,加入几滴
(2)方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是
(3)使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式
【问题2】灼烧绿矾的反应方程式:2(FeSO4?7H2O)
| ||
(1)装置Ⅰ中氯化钡溶液中可观察到现象
(2)装置Ⅱ中试剂为品红溶液,其作用是
(3)装置Ⅲ中试剂为NaOH溶液,其目的是
绿矾是一种重要的化工原料。
【问题1】绿矾晶体(FeSO4·7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质。为探究绿矾样品的变质情况,某化学兴趣小组的同学设计了下列实验方案。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)方案1:取少量溶液,加入几滴 试剂(写化学式),如果观察到的现象是溶液变血红色;实验结论:证明绿矾样品已被氧化。
(2)方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是 。实验结论:证明绿矾样品完全被氧化。
(3)使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 。
(4)要从FeSO4溶液中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、 过滤、自然干燥,在这一系列操作中没有用到的仪器有 (此空填序号)
| A.蒸发皿 | B.石棉网 | C.烧杯 | D.玻璃棒 |
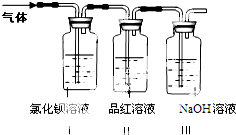
工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的气体产物中是否含有SO2和SO3,进行如下实验:将FeSO4高温分解产生的气体通入下图所示的装置中。请回答以下问题:

(1)装置I中氯化钡溶液中可观察到现象 。若氯化钡溶液足量,将最后所得沉淀过滤、洗涤、烘干后称重为2.33克,则灼烧绿矾的过程中转移了_________mol的电子。
(2)装置II中试剂为品红溶液,其作用是
(3)装置III中试剂为NaOH溶液,其作用是 。 查看习题详情和答案>>
绿矾是一种重要的化工原料。
【问题1】绿矾晶体(FeSO4·7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质。为探究绿矾样品的变质情况,某化学兴趣小组的同学设计了下列实验方案。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)方案1:取少量溶液,加入几滴 试剂(写化学式),如果观察到的现象是溶液变血红色;实验结论:证明绿矾样品已被氧化。
(2)方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是 。实验结论:证明绿矾样品完全被氧化。
(3)使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 。
(4)要从FeSO4溶液中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、 过滤、自然干燥,在这一系列操作中没有用到的仪器有 (此空填序号)
A.蒸发皿 B.石棉网 C.烧杯 D.玻璃棒
【问题2】灼烧绿矾的反应方程式:2(FeSO4·7H2O) Fe2O3+SO2↑+SO3↑+14H2O
工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的气体产物中是否含有SO2和SO3,进行如下实验:将FeSO4高温分解产生的气体通入下图所示的装置中。请回答以下问题:
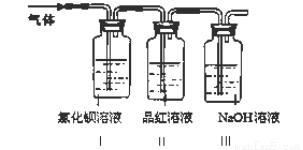
(1)装置I中氯化钡溶液中可观察到现象 。若氯化钡溶液足量,将最后所得沉淀过滤、洗涤、烘干后称重为2.33克,则灼烧绿矾的过程中转移了_________mol的电子。
(2)装置II中试剂为品红溶液,其作用是
(3)装置III中试剂为NaOH溶液,其作用是 。
查看习题详情和答案>>
【问题1】绿矾晶体(FeSO4·7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质。为探究绿矾样品的变质情况,某化学兴趣小组的同学设计了下列实验方案。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)方案1:取少量溶液,加入几滴 试剂(写化学式),如果观察到的现象是溶液变血红色;实验结论:证明绿矾样品已被氧化。
(2)方案2:取少量溶液,加入几滴酸性KMnO4溶液,如果观察到的现象是 。实验结论:证明绿矾样品完全被氧化。
(3)使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 。
(4)要从FeSO4溶液中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、 过滤、自然干燥,在这一系列操作中没有用到的仪器有 (此空填序号)
| A.蒸发皿 | B.石棉网 | C.烧杯 | D.玻璃棒 |
工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的气体产物中是否含有SO2和SO3,进行如下实验:将FeSO4高温分解产生的气体通入下图所示的装置中。请回答以下问题:

(1)装置I中氯化钡溶液中可观察到现象 。若氯化钡溶液足量,将最后所得沉淀过滤、洗涤、烘干后称重为2.33克,则灼烧绿矾的过程中转移了_________mol的电子。
(2)装置II中试剂为品红溶液,其作用是
(3)装置III中试剂为NaOH溶液,其作用是 。
甲醛溶液久置会产生分层现象,上层为无色油状液体,下层为水溶液,经测 定,上层物质为甲醛的聚合物(CH2O)![]() ,该分子中无醛基,且沸点比水高。已知:(CH2O)n→nCH2O(酸性环境中)
,该分子中无醛基,且沸点比水高。已知:(CH2O)n→nCH2O(酸性环境中)
(1)甲醛溶液置于空气中易被氧化,证明甲醛已被氧化的实验操作和现象是
。
(2)有人用下图a所示装置制取甲醛:烧瓶装(CH2O)n和6mol/L稀硫酸溶液,加热至沸腾,(CH2O)n分解,产生的甲醛气体被锥形瓶中的蒸馏水吸收,则冷凝管的进水方向为 (填“a”或“b”),从冷凝管中回流的液体是 ,导气管未插入锥形瓶液面下的原因是 。
常温下甲醛有毒,是致癌物和致畸形物之一。我国规定,居室空气中的甲醛的最高容许浓度为0.08mg/m3,某化学研究小组用如下方法测定居室中的甲醛的浓度(设空气中无其他还原性气体)。
测定原理:酸性高锰酸钾可氧化甲醛和草酸,其离子方程式为:
4MnO![]() +5HCHO+12H+==4Mn2++5CO2↑+11H2O
+5HCHO+12H+==4Mn2++5CO2↑+11H2O
( )MnO![]() +( )H2C2O4+( )H+→( )Mn2++( )CO2↑+( )H2O
+( )H2C2O4+( )H+→( )Mn2++( )CO2↑+( )H2O
测定装置如图b所示。
实验步骤:
(3)检查装置的气密性,如何检查装置的气密性?
。
(4)用 (填仪器名称)取足量酸性高锰酸钾溶液装入广口瓶中。
(5)打开a,关闭b,用注射器抽取100 mL新装修室内的空气,关闭a,打开b,再缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应,再如此重复多次,如果压人气体的速度过快,对测定结果如何影响?
。

(6)用草酸滴定广口瓶中的溶液,(填“要”或“不要”) 指示剂,终点的实验现象是 ,若高锰酸钾的浓度为c1,体积为V1mL,草酸的浓度为c2,消耗草酸溶液的平均体积为V2 mL,则甲醛的浓度是 mg/m3。(设抽取的空气体积为100mL)
查看习题详情和答案>>