摘要:13.碱金属元素的元素符号为 .随元素原子内核电荷数的递增.它们的密度将逐渐 .熔.沸点将逐渐 .硬度将逐渐 .
网址:http://m.1010jiajiao.com/timu3_id_243527[举报]
下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
(1)请写出上述元素d3+的核外电子排布式
(2)请比较y、h、i三种元素的第一电离能由大到小的顺序
(3)请写出e元素的原子价电子排布图
 ;
;
(4)ya3分子的电子式是
 ,其分子的空间构型是
,其分子的空间构型是
(5)b、e两种元素中,金属性较强的是
查看习题详情和答案>>
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||
1s222s2p63s23p63d5
1s222s2p63s23p63d5
;(2)请比较y、h、i三种元素的第一电离能由大到小的顺序
F>N>O
F>N>O
(写元素符号),其原因是同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但N元素2p电子达到半充满的稳定构型,所以其第一电离能大于O元素
同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但N元素2p电子达到半充满的稳定构型,所以其第一电离能大于O元素
.(3)请写出e元素的原子价电子排布图


(4)ya3分子的电子式是


三角锥
三角锥
,分子中y原子的原子轨道的杂化类型是sp3
sp3
.(5)b、e两种元素中,金属性较强的是
Mg
Mg
(填元素符号),写出能证明这一结论的一个实验事实氢氧化镁碱性大于氢氧化铝
氢氧化镁碱性大于氢氧化铝
.Ⅰ、下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);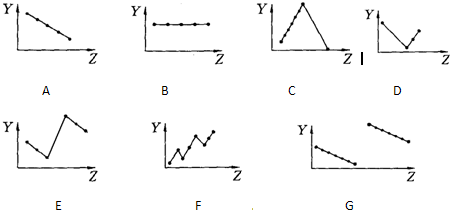
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数
(3)IA族碱金属元素单质熔点
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
(5)第二、三周期元素随原子序数递增原子半径的变化
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
查看习题详情和答案>>

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数
B
B
(2)第三周期元素的最高化合价C
C
(3)IA族碱金属元素单质熔点
A
A
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
E
E
(5)第二、三周期元素随原子序数递增原子半径的变化
G
G
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是
①
①
和④
④
;(2)质量数相等,但不能互称同位素的是
③
③
和⑥
⑥
;(3)中子数相等,但质子数不相等的是
④
④
和⑤
⑤
,②
②
和③
③
.阅读下表中的部分短周期主族元素的相关信息
请回答下列问题:
(1)描述Z元素在周期表中的位置:
(2)T、X、Y元素简单离子半径由大到小的顺序为:(填离子符号)
(3)已知1mol 化合物A与Na2SO3在溶液中发生反应时,转移2mol电子,写出该反应的离子方程式
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据上图提供的信息,试推断E氟
查看习题详情和答案>>
| 元素代号 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期金属元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
(1)描述Z元素在周期表中的位置:
第三周期第ⅦA族
第三周期第ⅦA族
(2)T、X、Y元素简单离子半径由大到小的顺序为:(填离子符号)
O2->Na+>Al3+
O2->Na+>Al3+
(3)已知1mol 化合物A与Na2SO3在溶液中发生反应时,转移2mol电子,写出该反应的离子方程式
SO32-+ClO-=SO42-+Cl-
SO32-+ClO-=SO42-+Cl-
.(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是
增大
增大
.②根据上图提供的信息,试推断E氟
>
>
E氧(填“>”“<”或“=”).Ⅰ、下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);
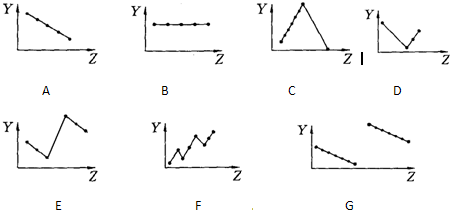
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数______ (2)第三周期元素的最高化合价______
(3)IA族碱金属元素单质熔点______
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径______
(5)第二、三周期元素随原子序数递增原子半径的变化______
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是______和______;
(2)质量数相等,但不能互称同位素的是______和______;
(3)中子数相等,但质子数不相等的是______和______,______和______.
查看习题详情和答案>>

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数______ (2)第三周期元素的最高化合价______
(3)IA族碱金属元素单质熔点______
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径______
(5)第二、三周期元素随原子序数递增原子半径的变化______
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是______和______;
(2)质量数相等,但不能互称同位素的是______和______;
(3)中子数相等,但质子数不相等的是______和______,______和______.
Ⅰ、下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);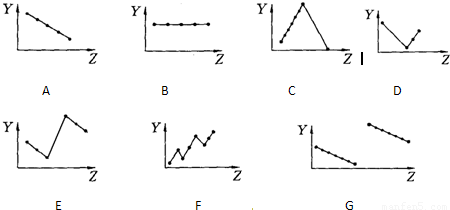
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数______ (2)第三周期元素的最高化合价______
(3)IA族碱金属元素单质熔点______
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径______
(5)第二、三周期元素随原子序数递增原子半径的变化______
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是______和______;
(2)质量数相等,但不能互称同位素的是______和______;
(3)中子数相等,但质子数不相等的是______和______,______和______.
查看习题详情和答案>>

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数______ (2)第三周期元素的最高化合价______
(3)IA族碱金属元素单质熔点______
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径______
(5)第二、三周期元素随原子序数递增原子半径的变化______
Ⅱ、在①126C ②3919K ③4020Ca ④136C ⑤147N ⑥4018Ar中:(用序号填空)
(1)互为同位素的是______和______;
(2)质量数相等,但不能互称同位素的是______和______;
(3)中子数相等,但质子数不相等的是______和______,______和______.
查看习题详情和答案>>