摘要:6].已知:4NH3+5O2=4NO+6H2O.若反应速率分别用...表示.则正确的关系是 A = B = C = D =
网址:http://m.1010jiajiao.com/timu3_id_243413[举报]
(2013?上海二模)某实验小组设计了下列装置进行氨的催化氧化实验.
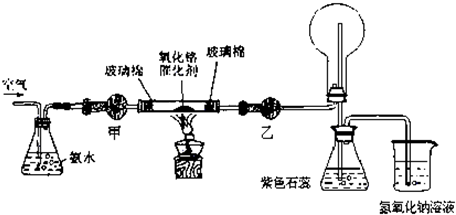
(1)常温下,氨水的浓度为1:1.5(28%的浓氨水和水的体积比)时实验现象明显,配制该浓度氨水的玻璃仪器有
(2)本实验用的干燥剂是碱石灰和无水氯化钙.则甲处是
(3)实验时,先将催化剂加热至红热,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明反应是
(4)实验前,烧杯中盛有200mL 1.000mol/L的 NaOH溶液,实验后测得烧杯中溶液的pH=13,且溶液质量比反应前增加了7.48g,则NaOH溶液吸收的NO和NO2的物质的量之比是
(5)实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生白烟.其原因可用化学方程式表示为:
(6)已知NH3和N2常压下的沸点分别为:-33.5℃和-195.8℃,据此推测这两种物质中,能做制冷剂的是
查看习题详情和答案>>

(1)常温下,氨水的浓度为1:1.5(28%的浓氨水和水的体积比)时实验现象明显,配制该浓度氨水的玻璃仪器有
量筒、烧杯、玻璃棒
量筒、烧杯、玻璃棒
.(2)本实验用的干燥剂是碱石灰和无水氯化钙.则甲处是
碱石灰
碱石灰
;乙处是无水氯化钙
无水氯化钙
.(3)实验时,先将催化剂加热至红热,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明反应是
放
放
(填“吸”或“放”)热反应;化学方程式为4NH3+5O2
4NO+6H2O
| ||
| 加热 |
4NH3+5O2
4NO+6H2O
.
| ||
| 加热 |
(4)实验前,烧杯中盛有200mL 1.000mol/L的 NaOH溶液,实验后测得烧杯中溶液的pH=13,且溶液质量比反应前增加了7.48g,则NaOH溶液吸收的NO和NO2的物质的量之比是
5:13
5:13
(设溶液的体积不变且忽略盐类的水解).(5)实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生白烟.其原因可用化学方程式表示为:
4NO+3O2+2H2O=4HNO3或2NO+O2=2NO2和3NO2+H2O=2HNO3+NO
或4NO2+O2+2H2O=4HNO3;
或4NO2+O2+2H2O=4HNO3;
4NO+3O2+2H2O=4HNO3或2NO+O2=2NO2和3NO2+H2O=2HNO3+NO
或4NO2+O2+2H2O=4HNO3;
、或4NO2+O2+2H2O=4HNO3;
NH3+HNO3=NH4NO3
NH3+HNO3=NH4NO3
.(6)已知NH3和N2常压下的沸点分别为:-33.5℃和-195.8℃,据此推测这两种物质中,能做制冷剂的是
NH3
NH3
(填分子式);能用来冷冻物质的是N2
N2
(填分子式).已知x为一种盐,A、C、D、F为无色气体,B在常温常压下为无色无味的液体,I和Y为中学化学中常见的单质,其中Y为气体,I为紫红色固体,E为黑色固体氧化物,L为蓝色沉淀.其中部分反应条件及产物已略去.

回答下列问题:
(1)C的电子式为
 ,L的化学式为
,L的化学式为
(2)写出反应①的化学方程式:
(3)写出反应②的离子方程式:
(4)已知M的水溶液呈酸性,用离子方程式解释原因:
(5)利用电解可提纯I物质,在该电解反应中电解质溶液是
(6)已知1 mol X在隔绝空气条件下分解产生的各产物的物质的量之比A:B:C:D=2:1:1:1,推测X的化学式为
查看习题详情和答案>>

回答下列问题:
(1)C的电子式为


Cu(OH)2
Cu(OH)2
.(2)写出反应①的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
反应①~④中属于氧化还原反应的是
| ||
| △ |
①②
①②
.(3)写出反应②的离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(4)已知M的水溶液呈酸性,用离子方程式解释原因:
NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
.(5)利用电解可提纯I物质,在该电解反应中电解质溶液是
CuSO4溶液
CuSO4溶液
;写出阴极的电极反应式:Cu2++2e-=Cu
Cu2++2e-=Cu
.(6)已知1 mol X在隔绝空气条件下分解产生的各产物的物质的量之比A:B:C:D=2:1:1:1,推测X的化学式为
(NH4)2C2O4
(NH4)2C2O4
.电镀含铬废水的处理方法较多.
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+、Fe3+和Al3+等,且酸性较强.为回收利用,通常采用如下流程处理:

已知:
(1)Cr(OH)3
NaCrO2
Na2CrO4
Na2Cr2O7
(2)Cu(OH)2能溶于氨水:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
请回答:(1)操作Ⅰ的名称
(2)滤渣Ⅰ的主要成分为
(3)加入试剂甲的目的
(4)废水处理流程中生成滤渣Ⅲ的离子方程式:
Ⅱ.酸性条件下,六价铬主要以Cr2O72-形式存在.工业上用以下方法处理处理含Cr2O72-的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准.
(5)电解时能否用Cu电极来代替Fe电极?
(6)已知某含Cr2O72-的酸性工业废水中铬元素的含量为104.5mg/L,处理后铬元素最高允许排放浓度为0.5mg/L.处理该废水1000m3并达到排放标准,至少消耗铁的质量为
查看习题详情和答案>>
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+、Fe3+和Al3+等,且酸性较强.为回收利用,通常采用如下流程处理:

已知:
(1)Cr(OH)3
| NaOH |
| Cl2 |
| 酸化 |
(2)Cu(OH)2能溶于氨水:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
请回答:(1)操作Ⅰ的名称
过滤
过滤
,上述操作Ⅰ、Ⅱ、Ⅲ相同,进行该实验操作所需要的主要玻璃仪器除烧杯、漏斗外,还有玻璃棒
玻璃棒
.(2)滤渣Ⅰ的主要成分为
Cu(OH)2、Fe(OH)3
Cu(OH)2、Fe(OH)3
(写化学式),试剂乙的名称氨水
氨水
.(3)加入试剂甲的目的
将Fe2+氧化成Fe3+
将Fe2+氧化成Fe3+
.(4)废水处理流程中生成滤渣Ⅲ的离子方程式:
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
.Ⅱ.酸性条件下,六价铬主要以Cr2O72-形式存在.工业上用以下方法处理处理含Cr2O72-的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准.
(5)电解时能否用Cu电极来代替Fe电极?
不能
不能
(填“能”或“不能”),理由是因阳极产生的Cu2+不能使Cr2O72-还原到低价态
因阳极产生的Cu2+不能使Cr2O72-还原到低价态
.(6)已知某含Cr2O72-的酸性工业废水中铬元素的含量为104.5mg/L,处理后铬元素最高允许排放浓度为0.5mg/L.处理该废水1000m3并达到排放标准,至少消耗铁的质量为
336
336
kg. 如图表示的是25℃时,难溶氢氧化物在不同pH下的溶解度(S/mol?L-1,假定该浓度为饱和溶液中阳离子的浓度).
如图表示的是25℃时,难溶氢氧化物在不同pH下的溶解度(S/mol?L-1,假定该浓度为饱和溶液中阳离子的浓度).请完成下列问题:
(1)pH=3时溶液中铜元素的主要存在形式是
Cu2+
Cu2+
.(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH
B
B
(填选项).A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
不能
不能
(填“能”或“不能”)通过调节溶液pH的方法来除去,理由是Co2+和Ni2+沉淀的pH范围相差太小
Co2+和Ni2+沉淀的pH范围相差太小
.(4)25℃下Ksp[Cu( OH )2]=
1.0×10-20
1.0×10-20
.(5)要使Cu(OH)2沉淀溶解,除了加酸之外,还可以加入氨水生成[Cu(NH3)4]2+,写出反应的离子方程式
Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
.(6)已知一些难溶物的溶度积常数如下表.
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-35 | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 |
FeS
FeS
填选项B
B
. A.NaOH B.FeS C.Na2S.
 4NO
(g)+6
H2O (g);该反应是一个可逆反应,正反应是放热反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是 ( )
4NO
(g)+6
H2O (g);该反应是一个可逆反应,正反应是放热反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是 ( )