网址:http://m.1010jiajiao.com/timu3_id_242518[举报]
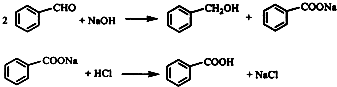
已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃).
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸.
③石蜡油沸点高于250℃
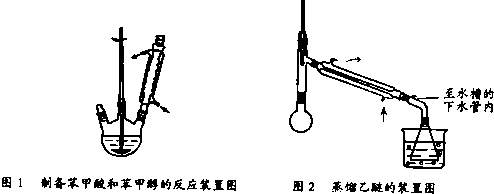
实验步骤如下:
①向图l 所示装置中加入8g氢氧化钠和30mL水,搅拌溶解.稍冷,加入10mL苯甲醛.开启搅拌器,调整转速,使搅拌平稳进行.加热回流约40min.
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温.反应物冷却至室温后,用乙醚萃取三次,每次
10mL.水层保留待用.合并三次萃取液,依次用5mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10mL水洗涤,分液水层弃去所得醚层进行实验③.
③将分出的醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞.将锥形瓶中溶液转入图2 所示蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必需改变加热方式,升温至140℃时应对水冷凝管冷凝方法调整,继续升高温度并收集203℃~205℃的馏分得产品A.
④实验步骤②中保留待用水层慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体.冷却,抽滤,得到粗产品,然后提纯得产品B.
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需
(2)饱和亚硫酸氢钠溶液洗涤是为了除去


(3)步骤③中无水硫酸镁是
(4)蒸馏除乙醚的过程中采用的加热方式为
(5)提纯产品B 所用到的实验操作为
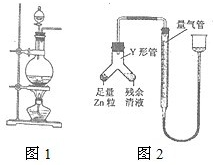 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示).(1)制备实验开始时,先检查装置气密性,接下来的操作依次是
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
制备反应会因盐酸浓度下降而停止.为测定已分离出过量MnO2后的反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量.
乙方案:与已知量CaCO3(过量)反应,称量剩余固体的质量.
丙方案:与足量Zn反应,测量生成的H2体积.
继而进行下列判断和实验:
(2)判定甲方案不可行,理由是
(3)乙方案的实验发现,固体中含有MnCO3,说明碳酸钙在水中存在
进行丙方案实验:装置如图2所示(夹持器具已略去).
(4)使Y形管中的残余清液与锌粒反应的正确操作是将
(5)反应完毕,每间隔1分钟读取气体体积,发现气体体积逐渐减小,直至不变.气体体积逐次减小的原因是
(排除装置和实验操作的影响因素).
(6)小组内又有同学提出还可采用酸碱中和滴定法测定残余液中盐酸的浓度,但还需经查阅资料知道:
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图所示)。

(1)制备实验开始时,先检查装置气密性,接下来的操作依次是__________(填序号)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
制备反应会因盐酸浓度下降而停止。为测定已分离出过量MnO2后的反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:与已知量CaCO3(过量)反应,称量剩余固体的质量。
丙方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:
(2)判定甲方案不可行,理由是______________________________________________________。
(3)乙方案的实验发现,固体中含有MnCO3,说明碳酸钙在水中存在__________________,测定的结果会:______________________(填“偏大”、“偏小”或“准确”)。
进行丙方案实验:装置如图所示(夹持器具已略去)。
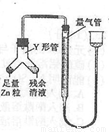
(4)使Y形管中的残余清液与锌粒反应的正确操作是将________转移到______中。
(5)反应完毕,每间隔1分钟读取气体体积,发现气体体积逐渐减小,直至不变。 气体体积逐次减小的原因是____________(排除装置和实验操作的影响因素)。
(6)小组内又有同学提出还可采用酸碱中和滴定法测定残余液中盐酸的浓度,但还需经查阅资料知道:________________________________________________________ 。
查看习题详情和答案>>
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如下图所示).

1.制备实验开始时,先检查装置气密性,接下来的操作依次是(填序号).
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
制备反应会因盐酸浓度下降而停止.为测定已分离出过量MnO2后的反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案∶
甲方案∶与足量AgNO3溶液反应,称量生成的AgCl质量.
乙方案∶与已知量CaCO3(过量)反应,称量剩余固体的质量.
丙方案∶与足量Zn反应,测量生成的H2体积.
继而进行下列判断和实验∶
2.判定甲方案不可行,理由是________.
3.乙方案的实验发现,固体中含有MnCO3,说明碳酸钙在水中存在________,测定的结果会∶(填“偏大”、“偏小”或“准确”).
进行丙方案实验∶装置如下图所示(夹持器具已略去).

4.使Y形管中的残余清液与锌粒反应的正确操作是将转移到________中.
5.反应完毕,每间隔1分钟读取气体体积,发现气体体积逐渐减小,直至不变.气体体积逐次减小的原因是________(排除装置和实验操作的影响因素).
6.小组内又有同学提出还可采用酸碱中和滴定法测定残余液中盐酸的浓度,但还需经查阅资料知道∶________.
(14分)实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下: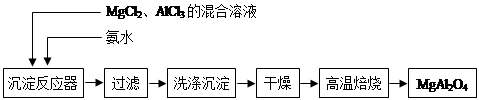
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式 。
(2)如图所示,过滤操作中的一处错误是 。判断流程中沉淀是否洗净所用的试剂是 。高温焙烧时,用于盛放固体的仪器名称是 。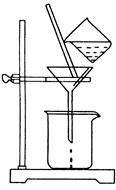
(3)在25℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴 加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式 (已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34。)
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。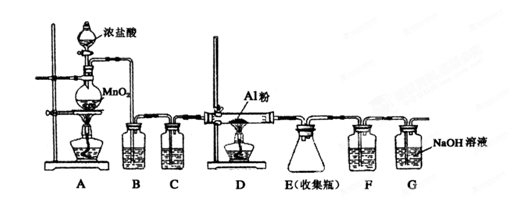
装置B中盛放饱和NaCl溶液,该装置的主要作用是 ;F中试剂的作用是 ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 。
(5)将Mg、Cu组成的1.96g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后的溶液中加入2 mol/L的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为 g。