摘要:下列反应达到平衡时.增大压强.平衡是否移动?向那个方向移动? ①2NO+O2(g)
网址:http://m.1010jiajiao.com/timu3_id_241752[举报]
(12分)在298K、100kPa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的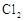 约有三分之一与水反应。请回答下列问题:
约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为______________________________________;
(2)估算该反应的平衡常数________________(列式计算,写明解题过程,否则不得分);
(3)在上述平衡体系中加入少量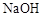 固体,平衡将向________移动;
固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将_______(填“增大”“减少”或“不变”),平衡将向_________移动。
(5)氯气溶于水达到饱和后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,c(H+)/c( )减小 )减小 |
| B.通入少量HCl,溶液漂白性增强 |
C.加入少量固体NaOH,一定有c(Na+)=c(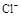 )+c( )+c( ) ) |
| D.加入少量CaCO3,溶液漂白性增强 |
(12分)在298K、100kPa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的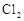 约有三分之一与水反应。请回答下列问题:
约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为______________________________________;
(2)估算该反应的平衡常数________________(列式计算,写明解题过程,否则不得分);
(3)在上述平衡体系中加入少量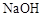 固体,平衡将向________移动;
固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将_______(填“增大”“减少”或“不变”),平衡将向_________移动。
(5)氯气溶于水达到饱和后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,c(H+)/c( )减小
)减小
B.通入少量HCl,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(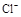 )+c(
)+c( )
)
D.加入少量CaCO3,溶液漂白性增强
查看习题详情和答案>>
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理.请回答下列问题:
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
;
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
查看习题详情和答案>>
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
3mol/L<c(B)<9mol/L
3mol/L<c(B)<9mol/L
;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是①③
①③
.①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
K=K1×K2
K=K1×K2
.(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
否
否
(填“是”或“否”)达到化学平衡状态,若未达到,向逆反应
逆反应
(填“正反应”或“逆反应”)方向进行.(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
正反应
正反应
(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则x<
<
0(填“>”或“<”). 右图是温度和压强对X+Y?2Z反应影响的示意图.图中纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )
右图是温度和压强对X+Y?2Z反应影响的示意图.图中纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )| A、X、Y、Z均为气态 | B、恒容时,混合气体的密度可作为此反应是否达到化学平衡的判断依据 | C、升高温度时v正增大,v逆减小,平衡向右移动 | D、使用催化剂Z的产率增加 |