题目内容
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理.请回答下列问题:
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
;
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
3mol/L<c(B)<9mol/L
3mol/L<c(B)<9mol/L
;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是①③
①③
.①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
K=K1×K2
K=K1×K2
.(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
否
否
(填“是”或“否”)达到化学平衡状态,若未达到,向逆反应
逆反应
(填“正反应”或“逆反应”)方向进行.(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
正反应
正反应
(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则x<
<
0(填“>”或“<”).分析:(1)若A完全转化为C,B取最小值,若C完全转化为反应物,B取最大值;改变条件重新达到平衡后体系中C的体积分数增大,可使平衡正向移动或增加C;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,已知的两个反应相加得到C(s)+CO2(g)?2CO(g),则K等于已知两个反应的平衡常数之积;
(3)2SO2+02?2S03
开始 1 1 0
转化0.8 0.4 0.8
转化80%后0.2 0.6 0.8
Qc=
=26.7>K;
(4)增大压强,平衡向气体体积缩小的方向移动;升高温度,平衡向吸热的方向移动.
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,已知的两个反应相加得到C(s)+CO2(g)?2CO(g),则K等于已知两个反应的平衡常数之积;
(3)2SO2+02?2S03
开始 1 1 0
转化0.8 0.4 0.8
转化80%后0.2 0.6 0.8
Qc=
| 0.82 |
| 0.22×0.6 |
(4)增大压强,平衡向气体体积缩小的方向移动;升高温度,平衡向吸热的方向移动.
解答:解:(1)可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L,
若A完全转化为C,消耗B为04mol/L,则B最小值为3mol/L,若C完全转化为反应物,生成2molB,则B的最大值为9mol/L,因反应为可逆反应,均不能完全转化,则B的浓度范围为3mol/L<c(B)<9mol/L;改变条件重新达到平衡后体系中C的体积分数增大,可使平衡正向移动或增加C,升高温度平衡正向移动,符合题意,而加压平衡逆向移动,使用催化剂平衡不移动,故选①③,
故答案为:3mol/L<c(B)<9mol/L;①③;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
,已知的两个反应相加得到C(s)+CO2(g)?2CO(g),则K等于已知两个反应的平衡常数之积,即K=K1×K2,故答案为:
;K=K1×K2;
(3)2SO2+02?2S03
开始 1 1 0
转化0.8 0.4 0.8
转化80%后0.2 0.6 0.8
Qc=
=26.7>K,没有达到平衡,平衡向逆反应方向移动,故答案为:否;逆反应;
(4)增大压强,平衡向气体体积缩小的方向移动,a+b>c+d,增大压强平衡向正反应方向移动;升高温度,平衡向吸热的方向移动,由升高温度,平衡向逆反应方向移动,则x<0,故答案为:正反应;<.
若A完全转化为C,消耗B为04mol/L,则B最小值为3mol/L,若C完全转化为反应物,生成2molB,则B的最大值为9mol/L,因反应为可逆反应,均不能完全转化,则B的浓度范围为3mol/L<c(B)<9mol/L;改变条件重新达到平衡后体系中C的体积分数增大,可使平衡正向移动或增加C,升高温度平衡正向移动,符合题意,而加压平衡逆向移动,使用催化剂平衡不移动,故选①③,
故答案为:3mol/L<c(B)<9mol/L;①③;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
(3)2SO2+02?2S03
开始 1 1 0
转化0.8 0.4 0.8
转化80%后0.2 0.6 0.8
Qc=
| 0.82 |
| 0.22×0.6 |
(4)增大压强,平衡向气体体积缩小的方向移动,a+b>c+d,增大压强平衡向正反应方向移动;升高温度,平衡向吸热的方向移动,由升高温度,平衡向逆反应方向移动,则x<0,故答案为:正反应;<.
点评:本题考查较综合,涉及化学平衡的影响因素、化学平衡的计算等,把握温度、压强对平衡的影响及可逆反应的特性、K的计算等为解答的关键,平衡常数K与反应的关系,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
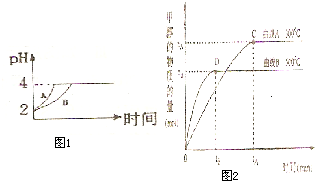 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题. 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: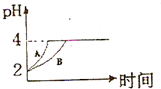 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是