摘要:在如图所示的电路中.R1.R2.R3和R4皆为定值电阻.R5为可变电阻.电源的电动势为E.内阻为r.设电流表A的读数为I.电压表V的读数为U.当R5的滑动触点向图中a端移动时 A.I变大.U变小 B.I变大.U变大 C.I变小.U变大 D.I变小.U变小
网址:http://m.1010jiajiao.com/timu3_id_238968[举报]
|
在如图所示的电路中,有一烧杯中盛有Ba(OH)2溶液,由滴管逐滴向烧杯中加H2SO4溶液至过量,则灯泡L和电流表
| |
A. |
L先亮后暗, |
B. |
L逐渐变暗, |
C. |
L先亮后暗, |
D. |
L先暗后亮, |
 50mL 0.5mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.请回答下列问题:
50mL 0.5mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.请回答下列问题:(1)烧杯间填满碎纸片的作用是
减少实验过程中的热量损失
减少实验过程中的热量损失
.(2)大烧杯上如不盖硬纸板,求得的中和热数值
偏小
偏小
(填“偏大”“偏小”“无影响”).(3)经测定,该中和反应放出的热量为Q kJ.则其热化学方程式为
HCl(aq)+NaOH(aq)=H2O(l)△H=-57.3kJ?mol-1
HCl(aq)+NaOH(aq)=H2O(l)△H=-57.3kJ?mol-1
.(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
偏小
偏小
(填“偏大”“偏小”“无影响”).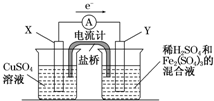 (2010?宝鸡一模)(2011?长春质检)金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)
(2010?宝鸡一模)(2011?长春质检)金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)(1)写出铜溶解于上述混合液的离子方程式
Cu+2Fe3+═Cu2++2Fe2+
Cu+2Fe3+═Cu2++2Fe2+
.(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是
0.64
0.64
g,溶液中的c(SO2- 4 |
0.5
0.5
mol/L.(3)若欲在如图所示的装置中发生(1)中的反应,请判断图中的正、负极,并选出适当的物质作电极,写出电极反应式,填在相应的表格中.
| 正、负极判断 | 电极材料 | 电极反应式 | |
| X极 | 负 负 |
铜 铜 |
Cu-2e-═Cu2+ Cu-2e-═Cu2+ |
| Y极 | 正 正 |
碳 碳 |
2Fe3++2e-═2Fe2+ 2Fe3++2e-═2Fe2+ |
 用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)玻璃搅拌棒能否用铁质搅拌棒代替?
不能
不能
(填“能”或“不能”),其原因是铁质搅拌棒易传热,散发热量,会使测出的温度偏低,所得中和热的测定值比理论值偏低
铁质搅拌棒易传热,散发热量,会使测出的温度偏低,所得中和热的测定值比理论值偏低
;(2)实验时氢氧化钠溶液的浓度要用0.55mol/L的原因是
要保证盐酸反应完全,以盐酸的量为准进行准确计算
要保证盐酸反应完全,以盐酸的量为准进行准确计算
;(3)实验中若改用60mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量
不相等
不相等
(填“相等”“不相等”),若实验操作均正确,则所求中和热相等
相等
(填“相等”“不相等”). 金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).(1)写出铜溶解于上述混合溶液的离子方程式
Cu+2Fe3+═Cu2++2Fe2+
Cu+2Fe3+═Cu2++2Fe2+
.(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是
0.64
0.64
g,溶液中的c(SO2- 4 |
0.3
0.3
mol/L.(3)若欲在如图所示的装置中发生(1)中的反应,则X极是
负极
负极
(正、负极),电极反应式Cu-2e-═Cu2+
Cu-2e-═Cu2+
.Y极的材料名称是碳(石墨、金、铂、银)
碳(石墨、金、铂、银)
,电极反应式2Fe3++2e-═2Fe2+
2Fe3++2e-═2Fe2+
.