摘要:在标准状况下.1mol下列物质所占的体积最小的是( ) A.铜 B.氢气 C.空气 D. CO2
网址:http://m.1010jiajiao.com/timu3_id_231368[举报]
(1)14.2g Na2SO4溶于水配成1L的溶液,则该Na2SO4溶液的物质的量的浓度为
(2)9.03×1023个CO2分子中含
查看习题详情和答案>>
0.1mol/L
0.1mol/L
,所含Na+的物质的量浓度为0.2mol/L
0.2mol/L
,SO42-的数目为0.1NA
0.1NA
.(2)9.03×1023个CO2分子中含
3mol
3mol
摩尔氧原子,在标准状况下其体积为33.6L
33.6L
,它与54
54
克H2O含有相同的氧原子数.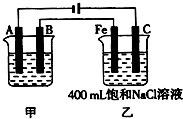 图为相互串联的甲、乙两电解池.试回答:
图为相互串联的甲、乙两电解池.试回答:(1)若甲电解池利用电解原理在铁上镀银,则A是
铁
铁
、填电极材料),电极反应式Ag++e-=Ag
Ag++e-=Ag
;B(要求同A)是银
银
,电极反应式Ag-e-=Ag+
Ag-e-=Ag+
,应选用的电解质溶液是AgNO3溶液
AgNO3溶液
.(2)乙电解池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈
红
红
色.C极附近呈浅黄绿色
浅黄绿色
色.(3)若甲电解池阴极增重4.32g,则乙槽中阳极上放出的气体在标准状况下的体积是
448
448
mL.(4)若乙电解池中剩余溶液仍为400mL,则电解后所得溶液中新生成溶质的物质的量浓度为
0.1
0.1
mol?L-1,溶液的pH等于13
13
.判断题(对的打√,错的打×)
(1)1mol氢中含有NA个氢原子
(2)1molCO2含有NA个氧原子
(3)1molH2O中含有1molH2和 1mol O
(4)在标准状况下,1mol水的体积约是22.4L
(5)1mol O2在20℃时的体积一定大于22.4L
(6)在标准状况下,0.5mol N2和1mol O2 的混合气体的体积约是33.6L
查看习题详情和答案>>
(1)1mol氢中含有NA个氢原子
×
×
(2)1molCO2含有NA个氧原子
×
×
(3)1molH2O中含有1molH2和 1mol O
×
×
(4)在标准状况下,1mol水的体积约是22.4L
×
×
(5)1mol O2在20℃时的体积一定大于22.4L
×
×
(6)在标准状况下,0.5mol N2和1mol O2 的混合气体的体积约是33.6L
√
√
. 电化学在工业生产中有广泛应用.
电化学在工业生产中有广泛应用.(一)如图1所示,水槽中试管内有一枚铁钉,放置数天观察,发现铁钉被腐蚀.
(1)若试管内液面上升,发生
吸氧
吸氧
腐蚀,电极反应为负极:Fe-2e-+2OH-═Fe(OH)2
Fe-2e-+2OH-═Fe(OH)2
;正极:O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
.(2)若试管内液面下降,则烧杯中的溶液呈
强酸
强酸
性,正极的电极反应为:2H++2e-═H2↑
2H++2e-═H2↑
.(二)如图2为相互串联的甲、乙两个电解池(电极都是惰性电极),请回答:
(1)写出甲电解池中的电解总反应方程式:
2CuSO4+2H2O═2Cu+O2↑+2H2SO4
2CuSO4+2H2O═2Cu+O2↑+2H2SO4
.(2)若甲槽阴极增重12.8g,则乙槽阳极放出气体为
Cl2
Cl2
,在标准状况下的体积为4.48L
4.48L
;检验该气体一般用湿润的淀粉-KI试纸,现象是试纸变蓝
试纸变蓝
,发生的反应是Cl2+2I-═I2+2Cl-
Cl2+2I-═I2+2Cl-
.(3)若乙槽剩余液体为400mL,则电解后得到碱液的物质的量浓度为
1mol/L
1mol/L
;电解过程中,乙槽溶液pH的变化为(“升高”、“降低”或“不变”)升高
升高
.