网址:http://m.1010jiajiao.com/timu3_id_210997[举报]
(1)草酸(H2C2O4)分解的化学方程式为:
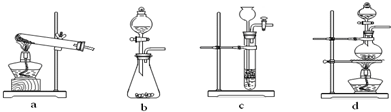
(2)某探究小组利用草酸分解产生的混合气体和铁锈反应来测定铁锈样品组成(假定铁锈中只有Fe2O3?nH2O
和Fe两种成份),实验装置如下图所示,请回答:
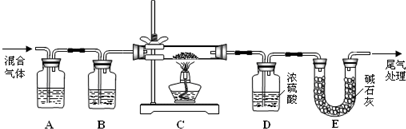
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是
②在点燃酒精灯之前应进行的操作是:(a)
③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量,硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=
④在本实验中,下列情况会使测定结果n偏大的是
a.缺少洗气瓶B b.缺少装置E
c.反应后固体是铁和少量Fe2O3 d.反应后固体是铁和少量Fe2O3?nH2O
(3)该探究小组还利用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
①请完成以下实验设计表(表中不要留空格):
(每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL,催化剂
| 实验 编号 |
实验目的 | T/K | 催化剂用量/g | C/mol?l-1 | |
| KMnO4 | H2C2O4 | ||||
| ① | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| ② | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| ③ | 323 | 0.5 | 0.01 | 0.1 | |
| ④ | 探究催化剂对反应速率的影响 | 0.1 | |||
②若要准确计算反应速率,该实验中还需测定溶液紫色消失所需要的时间.请你设计出通过测定褪色时间长短来判断浓度大小与反应速率关系的实验方案
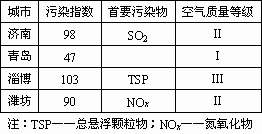
城市 污染指数 首要污染物 空气质量等级
济南 98 SO2 Ⅱ
青岛 47 Ⅰ
淄博 103 TSP Ⅲ
潍坊 90 NOx Ⅱ
注:TSP—总悬浮颗粒物;NOx—氮氧化物
(1)由上表可知,最容易出现酸雨的城市是________。
(2)悬浮颗粒不易沉降,它与空气中的SO2、O2接触时,SO2会部分转化为SO3,悬浮颗粒物所起的作用是________。(填序号)
A.氧化剂 B.还原剂
C.催化剂 D.吸附剂
(3)氮的氧化物也是大气污染物之一。目前,治理NO的方法是在一定条件下用氨把一氧化氮还原为氮气和水。科学家又设想,在相同条件下可采用价格比NH3更便宜的天然气来处理NO,可得到同样效果,写出该反应的化学方程式_________________________________________________________________________。
(4)某中等城市每年燃煤约3´106t,其含硫量按1.00%计算,若硫全部转化为SO2,SO2有60.0%转化为硫酸,相当于生成多少吨98.0%的硫酸?
(列式计算)
查看习题详情和答案>>
空气质量越来越受到人们的关注,下表是我省部分城市空气质量周报:
城市 污染指数 首要污染物 空气质量等级
济南 98 SO2 Ⅱ
青岛 47 Ⅰ
淄博 103 TSP Ⅲ
潍坊 90 NOx Ⅱ
注:TSP—总悬浮颗粒物;NOx—氮氧化物
(1)由上表可知,最容易出现酸雨的城市是________。
(2)悬浮颗粒不易沉降,它与空气中的SO2、O2接触时,SO2会部分转化为SO3,悬浮颗粒物所起的作用是________。(填序号)
A.氧化剂 B.还原剂
C.催化剂 D.吸附剂
(3)氮的氧化物也是大气污染物之一。目前,治理NO的方法是在一定条件下用氨把一氧化氮还原为氮气和水。科学家又设想,在相同条件下可采用价格比NH3更便宜的天然气来处理NO,可得到同样效果,写出该反应的化学方程式_________________________________________________________________________。
(4)某中等城市每年燃煤约3´106t,其含硫量按1.00%计算,若硫全部转化为SO2,SO2有60.0%转化为硫酸,相当于生成多少吨98.0%的硫酸?
(列式计算)
查看习题详情和答案>>
| |||||||||||||||||||||||||||||
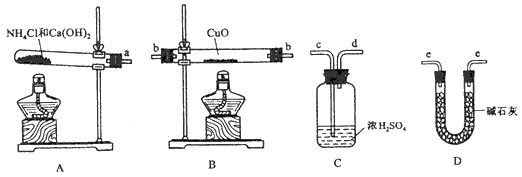
(1)氨气还原炽热氧化铜的化学方程式为____________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→__________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①CuO未完全起反应
② CuO不干燥
③CuO中混有不反应的杂质
④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定______和_____,或_____和______达到实验目的。