网址:http://m.1010jiajiao.com/timu3_id_209489[举报]

(1)写出下列元素符号:①
(2)画出原子的结构示意图:④




(3)在①~12元素中,金属性最强的元素是
(4)元素3、10、11的氢氧化物碱性由强到弱的顺序
(5)第三周期中有一种元素,其最高价氧化物的水化物与同周期其它元素最高价氧化物的水化物所属物质类型都不同,用离子方程式表示该水化物分别与烧碱溶液和稀硫酸的反应:
(6)与①和⑥都相邻的一种元素A,它有多种不同形态的单质,其中一种常用作原电池的电极,它与⑦的最高价氧化物的水化物浓溶液在加热时能反应,写出化学反应方程式:
| ||
| ||
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是
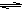 HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强
HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强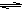 HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强
HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是
| 催化剂 |
| △ |
| 催化剂 |
| △ |
I.水是一种电解质,发生电离会产生电子总数相同的两种微粒,其电离方程式为
Ⅱ.在许多反应中H2O扮演不同的“角色”.请结合所学知识,写出有关反应的化学方程式或离子方程式.
(1)H2O参与置换反应,符合X+W→Y+V:
已知X和Y分别是短周期主族元素形成的两种单质,W、V是化合物.
①W是水,作还原剂,该反应的化学方程为
②V是水,化学方程式为
(2)水在氧化还原反应既不是氧化剂也不是还原剂:
A、B是中学化学常见的两种由短周期元素组成的有色气体,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,写出A、B与水反应的化学方程式:
①A+H2O
②B+H2O
(3)某物质化学式为NH5,常温下是固态,能与水剧烈反应放出两种气体.在NH5中的各原子均具有稀有气体的稳定结构,则下列对NH5与水的反应描述正确的是
A.NH5与水反应时,NH5是氧化剂 B.NH5与水反应时,NH5既是氧化剂又是还原剂
C.NH5与水反应时,NH5是还原剂 D.NH5与NH3溶于水后溶液均呈碱性.
请从给出的3道化学题中任选一题做答
1.[化学——选修化学与技术]
请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k__________(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是_________、_________(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
②分别写出燃料电池B中正极、负极上发生的电极反应
正极:_________;负极:_________;
③这样设计的主要节(电)能之处在于(写出2处)
___________________________、___________________________。
2.[化学——选修物质结构与性质]
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为_________,该元素的符号为_________;
(2)Y元素原子的价层电子的轨道表示式为_________,该元素的名称是_________;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________________________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是____________________________________;
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由____________________________________。
3.[化学——选修有机化学基础]
A~J均为有机化合物,它们之间的转化如下图所示:

实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气;
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1∶1∶1;
③G能使溴的四氯化碳溶液褪色;
④1 mol J与足量金属钠反应可放出22.4 L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为_________(不考虑立体异构),由A生成B的反应类型是_________反应;
(2)D的结构简式为___________________________;
(3)由E生成F的化学方程式为____________,E中的官能团有____________(填名称),与E具有相同官能团的E的同分异构体还有____________(写出结构简式,不考虑立体异构);
(4)G的结构简式为____________________________________;
(5)由I生成J的化学方程式为________________________。
查看习题详情和答案>>(15分)元素A的单质在氯碱工业中可用作电解槽的阳极材料。A在酸性溶液中被KMnO4氧化时,可生成橙黄色的AO4。在KCl存在下,AO4可被HCl还原成红色晶体K4[A2OCl10]。迄今已知只有两种金属四氧化物,AO4是稳定性较差的一种。A有两种重要的含氧酸钾盐B和C,其中元素A的含量分别为41.81%和49.50%。碱性介质中用Cl2氧化B可得到C;B在酸性介质中易歧化为AO2和C。
1.写出A的元素名称和符号。A在长式周期表中的第几周期,第几列?
2.写出AO4中A的杂化形态,AO4的几何构型。
3.写出B、C的化学式和反应方程式;
4.画出配合物(K4[A2OCl10])中阴离子的结构式。
5.写出六配位配合物ACl2(H2O)4+和ACl3(H2O)3的立体异构体?实验证实,后者的所有异构体经水解只转化成前者的某一种异构体Y。试画出Y的结构,并通过分析上述实验结果指出,配合物水解(取代)反应有什么规律?
查看习题详情和答案>>