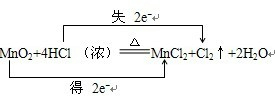
摘要:5.在反应MnO2+4HCl(浓)Cl2↑+Mn Cl2+2H2O中氧化剂与还原剂的物质的量比为( ) A.1:2 B.1:4 C.2:1 D.4:1
网址:http://m.1010jiajiao.com/timu3_id_207441[举报]
氧化还原是一类重要的反应.
(1)已知反应:①Cu+2Fe3+=Cu2++2Fe2+,②Cu2++Fe=Cu+Fe2+
反应①中还原剂是
(2)在反应MnO2+4HCl
MnCl2+Cl2↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是
(3)已知反应:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
①铜与稀硝酸反应的离子方程式是
②下列物质中,放到铜粉和稀硫酸中,能实现铜粉溶解的是
A.KNO3 B.K2SO4 C.Cu(NO3)2
③a g铜粉与足量的某浓度HNO3溶液完全反应后,产生V L(标准状况)气体,反应中消耗的HNO3的物质的量是
查看习题详情和答案>>
(1)已知反应:①Cu+2Fe3+=Cu2++2Fe2+,②Cu2++Fe=Cu+Fe2+
反应①中还原剂是
Cu
Cu
,两个反应中各种离子的氧化性从强到弱的顺序是Fe3+>Cu2+>Fe2+
Fe3+>Cu2+>Fe2+
.(2)在反应MnO2+4HCl
| ||
2.24L
2.24L
.(3)已知反应:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
①铜与稀硝酸反应的离子方程式是
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.②下列物质中,放到铜粉和稀硫酸中,能实现铜粉溶解的是
AC
AC
.A.KNO3 B.K2SO4 C.Cu(NO3)2
③a g铜粉与足量的某浓度HNO3溶液完全反应后,产生V L(标准状况)气体,反应中消耗的HNO3的物质的量是
(
+
)mol
| a |
| 32 |
| V |
| 22.4 |
(
+
)mol
.| a |
| 32 |
| V |
| 22.4 |
在反应MnO2+4HCl=MnCl2+Cl2+2H2O中,氧化剂是:
查看习题详情和答案>>
MnO2
MnO2
,还原剂是:HCl
HCl
,被氧化的物质是:HCl
HCl
,发生还原反应的物质是:MnO2
MnO2
.氧化产物是Cl2
Cl2
,还原产物是:MnCl2
MnCl2
当有0.5mol的Cl2生成时,反应中转移的电子数是:NA
NA
.