摘要:有一种活泼金属A.在一定条件下有如下的转化关系.已知B的焰色反应为黄色, F可使带火星的木条复燃,H能溶于盐酸生成一种能使澄清石灰水变浑浊的气体.请回答 下列问题: (1)分别写出下列化学方程式: A→C: , C→E: , D→E: . (2)分别写下列离子方程式: D→G: , G→H: , H能溶于盐酸生成一种能使澄清石灰水变浑浊的气体: .
网址:http://m.1010jiajiao.com/timu3_id_205640[举报]
 某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验
某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验| 序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
| 1 | Zn | Cu | 稀硫酸 | 有 |
| 2 | Zn | Zn | 稀硫酸 | 无 |
| 3 | Cu | C | 氯化钠溶液 | 有 |
| 4 | Mg | Al | 氢氧化钠溶液 | 有 |
(1)实验1中电流由
B
B
极流向A
A
极(填“A”或“B”)(2)实验4中电子由B极 流向A极,表明负极是
铝
铝
电极(填“镁”或“铝”)(3)实验3 表明
B
B
A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的(4)分析上表有关信息,下列说法不正确的是
A
A
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的二种金属(或其中一种非金属)
某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验
分析上述数据,回答下列问题:
(1)实验1中电流由______极流向______ 极(填“A”或“B”)
(2)实验4中电子由B极 流向A极,表明负极是______电极(填“镁”或“铝”)
(3)实验3 表明______A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是______
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的二种金属(或其中一种非金属)
 查看习题详情和答案>>
查看习题详情和答案>>
| 序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
| 1 | Zn | Cu | 稀硫酸 | 有 |
| 2 | Zn | Zn | 稀硫酸 | 无 |
| 3 | Cu | C | 氯化钠溶液 | 有 |
| 4 | Mg | Al | 氢氧化钠溶液 | 有 |
(1)实验1中电流由______极流向______ 极(填“A”或“B”)
(2)实验4中电子由B极 流向A极,表明负极是______电极(填“镁”或“铝”)
(3)实验3 表明______A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是______
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的二种金属(或其中一种非金属)
 查看习题详情和答案>>
查看习题详情和答案>>
(Ⅰ)下表是元素周期表的一部分,针对表中的①~⑥种元素,填写下列空白:
(1)在这些元素中,单质的化学性质最不活泼的是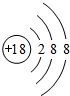
 .
.
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是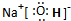
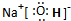 .
.
(3)最高价氧化物是两性氧化物的元素是
(4)①和④两元素分别形成的最高价氧化物中,熔点较高的是
(5)科学家借助元素周期表研究合成有特定性质的新物质,如在
(Ⅱ)化学与我们日常生活中的吃、穿、住、行、医关系密切,其中油脂、淀粉、蛋白质是我们食物中提供能量的主要物质.请按要求回答下列问题(填名称):
(1)油脂在酸性条件下水解的最终产物是
(2)淀粉水解的最终产物是
(3)蛋白质在一定条件下能发生水解反应,最终转化为
查看习题详情和答案>>
| 族周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ||||||||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑥ |
Ar
Ar
(填具体元素符号).原子结构示意图为

(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
HClO4
HClO4
,碱性最强的化合物的电子式是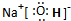
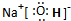
(3)最高价氧化物是两性氧化物的元素是
Al
Al
(填具体元素符号);写出它的氧化物与氢氧化钠反应的化学方程式Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.(4)①和④两元素分别形成的最高价氧化物中,熔点较高的是
SiO2
SiO2
(填具体化学式).(5)科学家借助元素周期表研究合成有特定性质的新物质,如在
金属与非金属交界处
金属与非金属交界处
寻找半导体材料.(Ⅱ)化学与我们日常生活中的吃、穿、住、行、医关系密切,其中油脂、淀粉、蛋白质是我们食物中提供能量的主要物质.请按要求回答下列问题(填名称):
(1)油脂在酸性条件下水解的最终产物是
高级脂肪酸
高级脂肪酸
和甘油
甘油
.(2)淀粉水解的最终产物是
葡萄糖
葡萄糖
.若要检验淀粉在淀粉酶作用下已经发生了水解,可取少量上述溶液加入新制氢氧化铜或银氨溶液
新制氢氧化铜或银氨溶液
,加热后再根据实验现象判断;若要检验淀粉没有完全水解,可取少量上述溶液加入几滴碘水
碘水
,应观察到出现蓝色.(3)蛋白质在一定条件下能发生水解反应,最终转化为
氨基酸
氨基酸
.X、Y、Z三种短周期元素,原子序数依次增大,其最外层电子数之和为15,它们分别是所在周期最活泼的金属或非金属元素.其中Y元素的单质在空气中可形成两种氧化物,其阴、阳离子个数比均为1:2.另有一常见金属W与常温下为液态的化合物A在一定条件下可发生如下变化:

请完成下列问题:
(1)、X、Y、Z三种元素的离子半径由大到小的顺序为
(2)、X、Z及第VIA族第一种元素的氢化物的沸点由高到低的顺序为
(3)、Y元素最高价氧化物对应水化物的电子式为
 .
.
(4)、W与Z的单质在一定条件下剧烈反应生成一种棕黄色的固体,将该固体溶于水得一黄色溶液,写出检验该溶液中金属离子的离子方程式(写一个)
(5)、B为黑色固体,在上述变化中,生成1molB转移电子
(6)、以(4)中的黄色溶液为电解质,W及另一种材料为电极构成原电池,5分钟后,W减轻10g,则另一种材料为
查看习题详情和答案>>

请完成下列问题:
(1)、X、Y、Z三种元素的离子半径由大到小的顺序为
Cl-F-Na+
Cl-F-Na+
(用离子符号表示).(2)、X、Z及第VIA族第一种元素的氢化物的沸点由高到低的顺序为
HF、HCl
HF、HCl
(用氢化物的分子式表示).(3)、Y元素最高价氧化物对应水化物的电子式为


(4)、W与Z的单质在一定条件下剧烈反应生成一种棕黄色的固体,将该固体溶于水得一黄色溶液,写出检验该溶液中金属离子的离子方程式(写一个)
Fe3++3SCN??Fe(SCN)3或Fe3++3OH?=Fe(OH)3↓
Fe3++3SCN??Fe(SCN)3或Fe3++3OH?=Fe(OH)3↓
.(5)、B为黑色固体,在上述变化中,生成1molB转移电子
8
8
mol.(6)、以(4)中的黄色溶液为电解质,W及另一种材料为电极构成原电池,5分钟后,W减轻10g,则另一种材料为
石墨或铜
石墨或铜
,电池总反应为Fe+2Fe3+=3Fe2+或Fe+2FeCl3=3FeCl2
Fe+2Fe3+=3Fe2+或Fe+2FeCl3=3FeCl2
.
X、Y、Z三种短周期元素,原子序数依次增大,其最外层电子数之和为15,它们分别是所在周期最活泼的金属或非金属元素.其中Y元素的单质在空气中可形成两种氧化物,其阴、阳离子个数比均为1:2.另有一常见金属W与常温下为液态的化合物A在一定条件下可发生如下变化:

请完成下列问题:
(1)、X、Y、Z三种元素的离子半径由大到小的顺序为 (用离子符号表示).
(2)、X、Z及第VIA族第一种元素的氢化物的沸点由高到低的顺序为 (用氢化物的分子式表示).
(3)、Y元素最高价氧化物对应水化物的电子式为 .
(4)、W与Z的单质在一定条件下剧烈反应生成一种棕黄色的固体,将该固体溶于水得一黄色溶液,写出检验该溶液中金属离子的离子方程式(写一个) .
(5)、B为黑色固体,在上述变化中,生成1molB转移电子 mol.
(6)、以(4)中的黄色溶液为电解质,W及另一种材料为电极构成原电池,5分钟后,W减轻10g,则另一种材料为 ,电池总反应为 . 查看习题详情和答案>>

请完成下列问题:
(1)、X、Y、Z三种元素的离子半径由大到小的顺序为 (用离子符号表示).
(2)、X、Z及第VIA族第一种元素的氢化物的沸点由高到低的顺序为 (用氢化物的分子式表示).
(3)、Y元素最高价氧化物对应水化物的电子式为 .
(4)、W与Z的单质在一定条件下剧烈反应生成一种棕黄色的固体,将该固体溶于水得一黄色溶液,写出检验该溶液中金属离子的离子方程式(写一个) .
(5)、B为黑色固体,在上述变化中,生成1molB转移电子 mol.
(6)、以(4)中的黄色溶液为电解质,W及另一种材料为电极构成原电池,5分钟后,W减轻10g,则另一种材料为 ,电池总反应为 . 查看习题详情和答案>>