摘要:6.如图1所示.在烧杯中装入50mL浓度为0.01mol·L的溶液.连接好导线.将开关闭合.然后向溶液中滴加0.2溶液至过量.则实验过程中烧杯内的液体导电能力变化为 A.先减弱.后增强 B.先增强.后减弱 C.一直增强 D.几乎不改变
网址:http://m.1010jiajiao.com/timu3_id_201390[举报]
 如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为( )
如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为( )
查看习题详情和答案>>
如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为( )
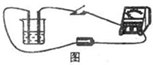
查看习题详情和答案>>
| A.先减弱,后增强 | B.先增强,后减弱 |
| C.一直增强 | D.几乎不改变 |

如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为( )

A.先减弱,后增强
B.先增强,后减弱
C.一直增强
D.几乎不改变
查看习题详情和答案>>

A.先减弱,后增强
B.先增强,后减弱
C.一直增强
D.几乎不改变
查看习题详情和答案>>
 如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为
如图所示,在烧杯中装入50mL浓度为0.01mol?L-1的Ba(OH)2溶液,连接好导线,将开关闭合,然后向Ba(OH)2溶液中滴加0.2mol?L-1H2SO4溶液至过量,则实验过程中烧杯内的液体导电能力变化为
- A.先减弱,后增强
- B.先增强,后减弱
- C.一直增强
- D.几乎不改变
 (1)50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热,回答下列问题:①从实验装置上看,图中尚缺少的一种玻璃用品是
环形玻璃搅拌棒
环形玻璃搅拌棒
.②大烧杯上如不盖硬纸板,求得的中和热数值将
偏小
偏小
(填“偏大”“偏小”或“无影响”).(2)酸碱中和滴定是中学化学常见实验.
某学校化学课外小组用0.2000mol?L-1盐酸滴定未知浓度的氢氧化钠溶液,试回答下列问题.
①滴定过程中,眼睛应注视
锥形瓶内溶液颜色的变化
锥形瓶内溶液颜色的变化
.②在铁架台上垫一张白纸,其目的是
便于观察锥形瓶内液体颜色的变化,减小滴定误差
便于观察锥形瓶内液体颜色的变化,减小滴定误差
.③根据下表数据,计算被测烧碱溶液的物质的量浓度是
0.4000
0.4000
mol?L-1.(保留四位有效数字)| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
a.观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果
偏高
偏高
.b.若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果
偏高
偏高
.