摘要:元素周期表中.在金属元素与非金属元素分界线附近.可以找到( ) A 作为催化剂的材料 B 航空航天工业中的耐高温合金材料 C 原子能工业上用的材料 D 电子工业上用的半导体材料
网址:http://m.1010jiajiao.com/timu3_id_198378[举报]
碱金属元素在科学研究与生产生活中有着非常广泛的用途。
(1)锂是最轻的金属,如果用锂做一架飞机,两个人就可以抬动。锂在元素周期表中的表示如图所示,填写以下空格。
①Li在元素周期表中的位置: 。
②6.941的意义: __________________________。
(2)光电管是利用碱金属铯受到光照射时能形成电流这一光电效应的性质制成的。
①完成铯的原子结构示意图: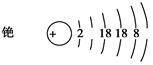
②下列有关铯的说法正确的是________。
| A.其单质在常温下与水反应不如钠剧烈, | B.其原子半径比钾原子半径小 |
| C.其氢氧化物的水溶液不能使氢氧化铝溶解, | D.其碳酸盐易溶于水 |
碱金属元素在科学研究与生产生活中有着非常广泛的用途。
(1)锂是最轻的金属,如果用锂做一架飞机,两个人就可以抬动。锂在元素周期表中的表示如图所示,填写以下空格。

①Li在元素周期表中的位置: 。
②6.941的意义: __________________________。
(2)光电管是利用碱金属铯受到光照射时能形成电流这一光电效应的性质制成的。
①完成铯的原子结构示意图:

②下列有关铯的说法正确的是________。
(1)锂是最轻的金属,如果用锂做一架飞机,两个人就可以抬动。锂在元素周期表中的表示如图所示,填写以下空格。

①Li在元素周期表中的位置: 。
②6.941的意义: __________________________。
(2)光电管是利用碱金属铯受到光照射时能形成电流这一光电效应的性质制成的。
①完成铯的原子结构示意图:

②下列有关铯的说法正确的是________。
| A.其单质在常温下与水反应不如钠剧烈, | B.其原子半径比钾原子半径小 |
| C.其氢氧化物的水溶液不能使氢氧化铝溶解, | D.其碳酸盐易溶于水 |
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)的CaO.
(1)Ca元素在周期表中位置是
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为
 ,A与Si形成的化合物为E.化合物E的空间构型为
,A与Si形成的化合物为E.化合物E的空间构型为
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为
查看习题详情和答案>>
(1)Ca元素在周期表中位置是
第四周期第ⅡA族
第四周期第ⅡA族
.(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为


正四面体
正四面体
.(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为
铁
铁
(填名称);检测Mn+的方法是Fe+3SCN-═Fe(SCN)3
Fe+3SCN-═Fe(SCN)3
(用离子方程式表达).元素周期表是学习物质结构与性质的重要工具.下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素.请用所给元素回答下列问题.
(1)Q元素在元素周期表中的位置

(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
(3)M、D两元素形成的化合物中含有的化学键类型是
(4)用表中所给元素组成反应物,用化学方程式说明元素Q和R非金属性的强弱:
查看习题详情和答案>>
| A | ||||||||||||||||||
| M | B | D | ||||||||||||||||
| G | H | Q | R | |||||||||||||||
| E | ||||||||||||||||||
第三周期ⅥA族
第三周期ⅥA族
,E元素原子结构示意图为

(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
S2->Cl->K+
S2->Cl->K+
.(3)M、D两元素形成的化合物中含有的化学键类型是
共价键
共价键
,其MD2分子的结构式:O=C=O
O=C=O
.(4)用表中所给元素组成反应物,用化学方程式说明元素Q和R非金属性的强弱:
H2S+C12=2HC1+S
H2S+C12=2HC1+S
;元素G、H的金属性强弱:2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
.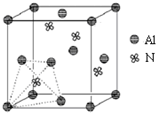 元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、磷化硼和砷化镓属于此列,如氮化铝晶体中每个Al原子与4个N原子相连,每个N原子也与4个Al原子相连,晶胞如右图所示.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层;砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%.试回答下列问题:
元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、磷化硼和砷化镓属于此列,如氮化铝晶体中每个Al原子与4个N原子相连,每个N原子也与4个Al原子相连,晶胞如右图所示.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层;砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%.试回答下列问题:(1)下列离子中最外层电子数不为8的是
D
D
(选填序号).A.P3- B.Al3+ C.Ti4+ D.Ga3+
(2)下列说法正确的是
BC
BC
(选填序号).A.硼和镓都属于S区元素,磷、砷属于P区元素
B.第一电离能:As>Ga Mg>Al
C.根据等电子体原理,砷化镓、磷化硼的晶胞与氮化铝晶体相同且类似于单晶硅
D.NH3沸点高于AsH3,其原因是NH3分子中共价键强度较大
(3)砷化镓可由(CH3)3Ga和AsH3反应得到,该反应在700℃进行,反应的化学方程式为
(CH3)3Ga+AsH3
GaAs+3CH4
| 700℃ |
(CH3)3Ga+AsH3
GaAs+3CH4
;| 700℃ |
下列有机分子中碳原子的杂化方式与(CH3)3Ga分子中Ga原子的杂化方式相同的是
BDE
BDE
.(填序号)A.CH4B.CH2=CH2C.CH≡CH D.HCHO E.

(4)请画出三溴化磷分子的路易斯结构式


非极性
非极性
(填“极性”“非极性”)分子.