摘要:14.一定物质的量的CO2和NaOH反应.所得溶液中含Na2CO3与NaHCO3的物质的量之比为 3:5.则参加反应的CO2和NaOH的物质的量之比为 A.1:2 B.8:11 C.8:13 D.3:5
网址:http://m.1010jiajiao.com/timu3_id_198108[举报]
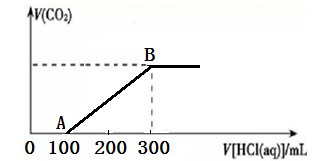
 将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).
将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).(1)O点溶液中所含溶质的化学式为
NaOH、Na2CO3
NaOH、Na2CO3
,(2)O到a点发生反应的离子方程式:
H++OH-=H2O、CO32-+H+=HCO3-
H++OH-=H2O、CO32-+H+=HCO3-
.(3)标准状况下通入CO2气体的体积为
44.8
44.8
L,NaOH溶液的物质的量浓度为2.5
2.5
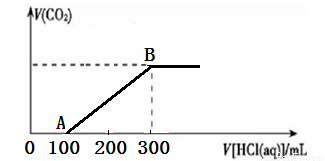
mol?L-1.将一定量的CO2气体通入2 L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).

(1)O点溶液中所含溶质的化学式为_____ ________,
(2)O到a点发生反应的离子方程式:_______________________________________.
(3) 标准状况下通入CO2气体的体积为__ L, NaOH溶液的物质的量浓度为____mol·L-1.
查看习题详情和答案>>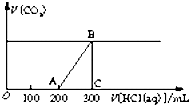 向200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.(1)此时溶液的溶质如果是单一成分,可能是
Na2CO3或NaHCO3
Na2CO3或NaHCO3
;如果是多种成分,可能是NaOH和Na2CO3或Na2CO3和NaHCO3
NaOH和Na2CO3或Na2CO3和NaHCO3
.(2)在上述所得溶液中,逐滴缓慢滴加2mol?L-1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:
①加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式
OH-+H+═H2O、CO32-+H+═HCO3-
OH-+H+═H2O、CO32-+H+═HCO3-
.②B点时,反应所得溶液中溶质的物质的量浓度是
1.2 mol?L-1
1.2 mol?L-1
(溶液体积的变化忽略不计).