网址:http://m.1010jiajiao.com/timu3_id_195872[举报]
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
|
物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
溶度积 |
2.8×10–9 |
6.8×10–6 |
5.5×10–6 |
1.8×10–11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为 (填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是 ;如果不能直接投入,应将贝壳作何处理,试写出化学方程式 。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为 (填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他 (填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是 (用离子方程式表示)。
(3)已知海水中镁离子浓度为1.8×10–3mol·L–1,则要使镁离子产生沉淀,溶液的PH最低应为 。
查看习题详情和答案>>
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10–9 | 6.8×10–6 | 5.5×10–6 | 1.8×10–11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为 (填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是 ;如果不能直接投入,应将贝壳作何处理,试写出化学方程式 。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为 (填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他 (填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是 (用离子方程式表示)。
(3)已知海水中镁离子浓度为1.8×10–3mol·L–1,则要使镁离子产生沉淀,溶液的PH最低应为 。 查看习题详情和答案>>
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10–9 | 6.8×10–6 | 5.5×10–6 | 1.8×10–11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为 (填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是 ;如果不能直接投入,应将贝壳作何处理,试写出化学方程式 。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为 (填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他 (填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是 (用离子方程式表示)。
(3)已知海水中镁离子浓度为1.8×10–3mol·L–1,则要使镁离子产生沉淀,溶液的PH最低应为 。
从海水中提取镁是世界各国获得镁的主要来源,下表是制镁过程中涉及的几种物质的溶度积,根据你所学的知识回答下列问题:
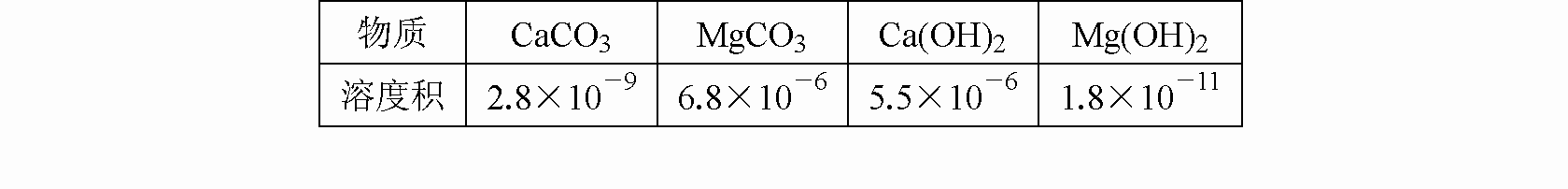
(1)从海水中提到镁时,往往会用到贝壳(主要成分是碳酸钙),你认为能否将贝壳研磨成粉末后直接投入海水中去获得含有镁元素的化合物?________(填“能”或“否”),其理由是________;如果不能直接投入,应将贝壳如何处理才能投入海水中,试写出有关贝壳处理过程中涉及的反应的化学方程式:________.
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用纯碱代替,你认为可否得到Mg(OH)2沉淀?________(填“能”或“否”).在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他能否将Mg2+转化为Mg(OH)2沉淀?________(填“能”或“否”),理由是________.
(3)常温下,已知某地海水中镁离子的浓度为1.8×10-3 mol/L,要使镁离子产生沉淀,溶液的pH值最低应为________.
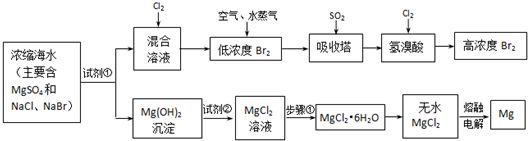
请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的1/3,主要方法就是上述流程中的空气吹出法.
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是
(2)吸收塔中反应的离子方程式是
由(1)、(2)可知,SO2、Cl2、Br2 三种物质氧化性由强到弱的顺序是
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的.
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
(2)加入试剂②后反应的离子方程式是
(3)步骤①包括加热、蒸发、冷却、结晶、
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
| ||
| ||
Ⅲ.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸.生产方法是:
①将氯化镁晶体(MgCl2?6H2O)加热到523℃以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体.
②将两种气体冷却至室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸.
(1)MgCl2?6H2O在523℃以上分解的化学方程式是
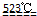 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑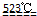 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑(2)现用1mol MgCl2?6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水