摘要:25实验室制取氯气时: (1)所用仪器:-----------------------------------------------------------------------, (2)反应原理:-----------------------------------------------------.该反应的还原剂是-----------, (3)实验开始前要对装置进行------------.方法是-------------------------------------------, (4)制取装置最后一部分用----------吸收多余气体.原因--------------.所发生的反应---------------------------------------------,能否用Na2CO3溶液吸收多余气体-----------26.完成相关气体制备反应方程式: (1)氨气的实验室制备反应式:------------------------------------------------, (2)二氧化碳的实验室制备反应式:------------------------------------------, (3)氧气的实验室制备反应式:------------------------------------------------.
网址:http://m.1010jiajiao.com/timu3_id_194809[举报]
实验室有某氯化铁与氯化亚铁的混合物.现要测定其中铁元素的质量分数,实验按以下步骤进行:

I.请根据上面流程,圆答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(2)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2
(3)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
×100%
×100%.
II.有同学提出,还可以采用以下方法来测定:

(4)在量取待测液和滴定过程中需要用到的滴定管是
A.一支酸式滴定管和一支碱式滴定管 B两支酸式滴定管 C两支碱式滴定管
(5)滴定终点的现象为
(6)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
(已知酸性条件下MnO4-被还原为Mn2+)
(7)在试验过程中,下列操作可能造成铁元素的质量分数偏高的是
A.溶解样品时用稀盐酸代替稀硫酸
B.用铁单质做还原剂
C.量取滤液时未润洗对应滴定管
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液.
查看习题详情和答案>>

I.请根据上面流程,圆答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
250ml容量瓶
250ml容量瓶
、胶头滴管
胶头滴管
(填仪器名称)(2)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2
小于0.1g
小于0.1g
,则视为灼烧充分;灼烧样品所需要的仪器有酒精灯、三脚架、坩埚
坩埚
、泥三角
泥三角
、玻璃棒
玻璃棒
、坩埚钳.(3)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
| 1120(W2-W1) |
| 160a |
| 1120(W2-W1) |
| 160a |
II.有同学提出,还可以采用以下方法来测定:

(4)在量取待测液和滴定过程中需要用到的滴定管是
B
B
(填番号)A.一支酸式滴定管和一支碱式滴定管 B两支酸式滴定管 C两支碱式滴定管
(5)滴定终点的现象为
当滴入最后一滴试液时,锥形瓶内溶液颜色变为紫红色且半分钟内不褪色
当滴入最后一滴试液时,锥形瓶内溶液颜色变为紫红色且半分钟内不褪色
;(6)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
| 14bc |
| 5a |
| 14bc |
| 5a |
(7)在试验过程中,下列操作可能造成铁元素的质量分数偏高的是
ABE
ABE
(填番号)A.溶解样品时用稀盐酸代替稀硫酸
B.用铁单质做还原剂
C.量取滤液时未润洗对应滴定管
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液.
实验室有某氯化铁与氯化亚铁的混合物.现要测定其中铁元素的质量分数,实验按以下步骤进行:
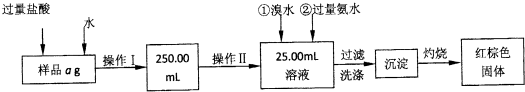
I.请根据上面流程,圆答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有______、______(填仪器名称)
(2)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2______,则视为灼烧充分;灼烧样品所需要的仪器有酒精灯、三脚架、______、______、______、坩埚钳.
(3)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是______.
II.有同学提出,还可以采用以下方法来测定:
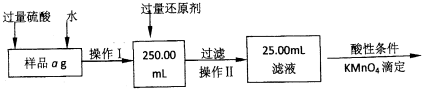
(4)在量取待测液和滴定过程中需要用到的滴定管是______(填番号)
A.一支酸式滴定管和一支碱式滴定管 B两支酸式滴定管 C两支碱式滴定管
(5)滴定终点的现象为______;
(6)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是______(已知酸性条件下MnO4-被还原为Mn2+)
(7)在试验过程中,下列操作可能造成铁元素的质量分数偏高的是______(填番号)
A.溶解样品时用稀盐酸代替稀硫酸
B.用铁单质做还原剂
C.量取滤液时未润洗对应滴定管
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液.
查看习题详情和答案>>
碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl?)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
开始沉淀pH | 4.2 | 5.8 | 1.2 |
完全沉淀pH | 6.7 | 8.3 | 3.2 |
①氯酸钠的作用是???????????? ;
②反应A后调节溶液的pH范围应为?????????????????????????? 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净????????????????????? 。
④造成蓝绿色产品中混有CuO杂质的原因是???????????????????? 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
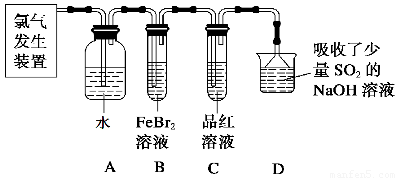
①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏的有??? ????????? ????? 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 ????????? ?? 。此时B装置中发生反应的离子方程式是___________?????????????? _____。
③写出A溶液中具有强氧化性微粒的化学式????????? ??????????????????? ?? 。若向A溶液中加入NaHCO3粉末,会观察到的现象是????????????????????? 。
查看习题详情和答案>>
碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl?)制备碱式碳酸铜,其制备过程如下:
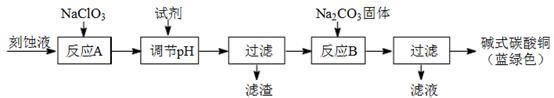
已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
①氯酸钠的作用是 ;
②反应A后调节溶液的pH范围应为 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净? 。
④造成蓝绿色产品中混有CuO杂质的原因是 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
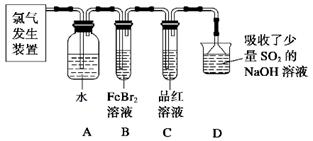
①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏有 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 。此时B装置中发生反应的离子方程式是 。
③写出A溶液中具有强氧化性微粒的化学式 。若向A溶液中加入NaHCO3粉末,会观察到的现象是 。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl?)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
②反应A后调节溶液的pH范围应为 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净? 。
④造成蓝绿色产品中混有CuO杂质的原因是 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。

①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏有 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 。此时B装置中发生反应的离子方程式是 。
③写出A溶液中具有强氧化性微粒的化学式 。若向A溶液中加入NaHCO3粉末,会观察到的现象是 。