摘要:① Mg(OH)2 理由略 ② 略 ③ 1.9g , 2.67g , 5.2g ④130mL
网址:http://m.1010jiajiao.com/timu3_id_194014[举报]
某化学兴趣小组的同学通过实验比较等体积(200mL)0.55mol/L硫酸、1.1mol/L盐酸、1.1mol/L醋酸分别与过量金属反应生成氢气的速率请你协助完成如下实验,并回答相关问题.

(1)实验用品:仪器(略)、药品(除给定的三种酸溶液外,在Na、Mg、Fe三种金属中选择最合适的一种,并说明理由).选择的金属是
(2)实验原理:(用离子方程式表示)
(3)甲同学设计的实验装置,乙同学认为该装置不能控制三个反应在同一时间发生,并作了相应的改进.你认为乙同学改进的措施是:
(4)按改进后的装置进行实验,实验中HCl与金属反应产生H2质量随时间变化的关系见图一,计算实验在80-120s范围内HCl的平均反应速率
(5)请在答题卡的框图中,画出HAc、H2SO4与金属反应产生H2质量随时间变化关系的预期结果示意图.
(6)量筒的规格由
(7)对盐酸和醋酸反应图象的异同,你的解释是
查看习题详情和答案>>

(1)实验用品:仪器(略)、药品(除给定的三种酸溶液外,在Na、Mg、Fe三种金属中选择最合适的一种,并说明理由).选择的金属是
Mg
Mg
,不选其它两种金属的理由是由于Na太活泼,能和水反应产生氢气,影响实验结论;Fe与酸反应的速率较慢,实验时间较长
由于Na太活泼,能和水反应产生氢气,影响实验结论;Fe与酸反应的速率较慢,实验时间较长
.(2)实验原理:(用离子方程式表示)
2H++Mg=H2↑+Mg2+、2CH3COOH+Mg=H2↑+Mg2++2CH3COO-
2H++Mg=H2↑+Mg2+、2CH3COOH+Mg=H2↑+Mg2++2CH3COO-
.(3)甲同学设计的实验装置,乙同学认为该装置不能控制三个反应在同一时间发生,并作了相应的改进.你认为乙同学改进的措施是:
同时用分液漏斗分别向烧瓶中加入酸液
同时用分液漏斗分别向烧瓶中加入酸液
.(4)按改进后的装置进行实验,实验中HCl与金属反应产生H2质量随时间变化的关系见图一,计算实验在80-120s范围内HCl的平均反应速率
0.00375mol/(L.min)
0.00375mol/(L.min)
(忽略溶液体积变化,写出计算过程).(5)请在答题卡的框图中,画出HAc、H2SO4与金属反应产生H2质量随时间变化关系的预期结果示意图.
(6)量筒的规格由
酸溶液的体积
酸溶液的体积
决定.(7)对盐酸和醋酸反应图象的异同,你的解释是
醋酸中存在电离平衡,反应开始时c(H+)小于盐酸,故反应速率也小于盐酸.由于醋酸、盐酸最终提供的H+的物质的量相等,故最后的得到H2体积相等.
醋酸中存在电离平衡,反应开始时c(H+)小于盐酸,故反应速率也小于盐酸.由于醋酸、盐酸最终提供的H+的物质的量相等,故最后的得到H2体积相等.
.
在氮的化合物中,有一类盐叫亚硝酸盐.如亚硝酸钠(NaNO2)等.它们广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂;它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐食用的事件.
某同学查阅有关资料,了解到以下相关信息:
亚硝酸及亚硝酸盐的资料:
(1)HNO2是一种弱酸(比醋酸略强),且不稳定,易分解生成NO和NO2
(2)HNO2能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把氧化成I2
(3)AgNO2种难溶于水易溶于酸的化合物
(4)NaNO2制备:
2NaOH+NO+NO2═2NaNO2+H2O
2NO2+2NaOH═NaNO3+NaNO2+H2O
2NaNO3
2NaNO2+O2↑
试回答下列问题:
(1)人体正常的血红蛋白中应含Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是 .
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(2)下列方法中,不能用来区别NaNO2和NaCl的是 .
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
D.分别在这两种溶液中滴加甲基橙
(3)为了测定某样品中NaNO2的含量,可以使用标准KMnO4溶液进行滴定,试回答:
①KMnO4溶液在滴定过程中作 (填“氧化剂”“还原剂”),该滴定过程 (填“要”或“不要”)另加指示剂.
②若滴定终点读数时目光俯视,则所得结果 (填“偏大”“偏小”“无影响”).
(4)某同学在家中欲进行鉴别NaCl与NaNO2的实验,但他家中只有浓醋酸,请问该实验能否成功?说明理由.
(5)现有氮的三种常见氧化物组成的混和气体44.8L(体积已换算成标准状态),其中N2O4、NO体积分数都为20%.
①将该气体通入适量的NaOH溶液中恰好反应,则溶液中NaNO2的质量是 g;
②反应后的溶液蒸干灼烧则NaNO2物质的量 mol.
查看习题详情和答案>>
某同学查阅有关资料,了解到以下相关信息:
亚硝酸及亚硝酸盐的资料:
(1)HNO2是一种弱酸(比醋酸略强),且不稳定,易分解生成NO和NO2
(2)HNO2能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把氧化成I2
(3)AgNO2种难溶于水易溶于酸的化合物
(4)NaNO2制备:
2NaOH+NO+NO2═2NaNO2+H2O
2NO2+2NaOH═NaNO3+NaNO2+H2O
2NaNO3
| ||
试回答下列问题:
(1)人体正常的血红蛋白中应含Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(2)下列方法中,不能用来区别NaNO2和NaCl的是
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
D.分别在这两种溶液中滴加甲基橙
(3)为了测定某样品中NaNO2的含量,可以使用标准KMnO4溶液进行滴定,试回答:
①KMnO4溶液在滴定过程中作
②若滴定终点读数时目光俯视,则所得结果
(4)某同学在家中欲进行鉴别NaCl与NaNO2的实验,但他家中只有浓醋酸,请问该实验能否成功?说明理由.
(5)现有氮的三种常见氧化物组成的混和气体44.8L(体积已换算成标准状态),其中N2O4、NO体积分数都为20%.
①将该气体通入适量的NaOH溶液中恰好反应,则溶液中NaNO2的质量是
②反应后的溶液蒸干灼烧则NaNO2物质的量
Ⅰ、铜器长期暴露在潮湿空气中,它的表层往往含有“铜绿”(碱式碳酸铜),它受热易分解,为了从铜绿中制得铜,并测定铜绿在混合物中的质量分数,把铜绿样品放在试管中,与通入的纯净氢气在加热条件下发生反应,实验装置如图1,请回答下列有关问题.
(1)A处应选用图2装置中的(填写编号)
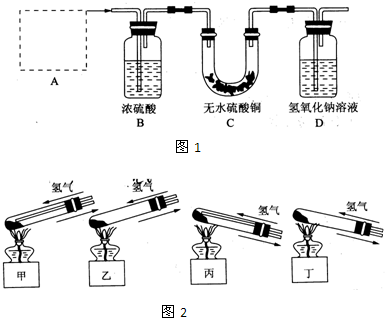
(2)反应开始前,对整个实验装置必须进行的操作是称量样品质量、检查装置的气密性和
(3)要测定铜绿在混合物中的质量分数,除需要知道样品质量外还需测定的实验数据是实验前后装置D质量.
(4)为使实验更准确,可采取的措施是
Ⅱ、10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为
(1)只要在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,则
A.Ba(OH)2溶液 B.BaC12溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
查看习题详情和答案>>
(1)A处应选用图2装置中的(填写编号)
丙
丙
(铁架台已省去),选用的理由是①因反应有水生成,试管口应略低于试管底部,防止冷凝水倒流到试管底部而使试管炸裂
因反应有水生成,试管口应略低于试管底部,防止冷凝水倒流到试管底部而使试管炸裂
;②通入氢气的导气管应伸入到试管底部,有利于将试管中的空气排净.
(2)反应开始前,对整个实验装置必须进行的操作是称量样品质量、检查装置的气密性和
称量装置D(含氢氧化钠溶液)的质量
称量装置D(含氢氧化钠溶液)的质量
;反应进行时,应先通氢气
通氢气
再加热
加热
;实验过程中,观察到试管中固体颜色变化为固体由绿色变黑色,最后变成光亮的红色
固体由绿色变黑色,最后变成光亮的红色
.(3)要测定铜绿在混合物中的质量分数,除需要知道样品质量外还需测定的实验数据是实验前后装置D质量.
(4)为使实验更准确,可采取的措施是
在D装置后加一个盛有碱石灰的球形干燥管
在D装置后加一个盛有碱石灰的球形干燥管
.Ⅱ、10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
.乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于
大于
(填“大小”或“小于”)NaHCO3.丙同学认为甲、乙的判断都不充分.丙认为:(1)只要在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,则
乙
乙
(填“甲”或“乙”)判断正确.试剂X是B
B
(填序号).A.Ba(OH)2溶液 B.BaC12溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则
甲
甲
(填“甲”或“乙”)判断正确.(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
乙
乙
(填“甲”或“乙”)判断是错误的,理由是常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
.实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):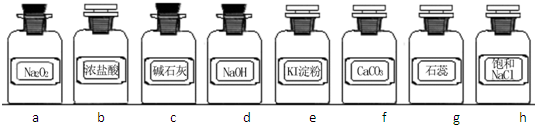
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式 .
(2)下列装置组合最合理的是 (填序号,需考虑实验结束撤除装置时残留有害气体的处理).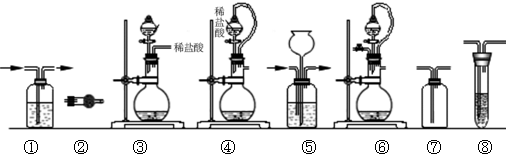
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为: .
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ,
② .
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一? (填“是”或“否”);
理由是 .
查看习题详情和答案>>

(1)写出用Na2O2与浓盐酸制备氯气的化学方程式
(2)下列装置组合最合理的是

| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③、⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④、⑥ | ⑤ | ⑧/g | ① |
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?
理由是
有一瓶溶液只含Cl-、CO32-、SO42-、Na+、NH4+、K+、Mg2+ 七种离子中的某几种.经如下实验:
①原溶液加入过量NaOH溶液,产生白色沉淀;
②将①所得溶液加热,放出使湿润的红色石蕊试纸变蓝的气体;
③原溶液中加BaCl2溶液不产生沉淀.
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解.
回答下列问题:
(1)试分析原溶液中一定含有的离子是 ,一定不含有的离子是 .
(2)请写出实验①、②、④有关反应的离子方程式:
①产生白色沉淀 ;
②产生气体 ;
④产生白色沉淀 .
(3)有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”) ,并说明理由 .
查看习题详情和答案>>
①原溶液加入过量NaOH溶液,产生白色沉淀;
②将①所得溶液加热,放出使湿润的红色石蕊试纸变蓝的气体;
③原溶液中加BaCl2溶液不产生沉淀.
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解.
回答下列问题:
(1)试分析原溶液中一定含有的离子是
(2)请写出实验①、②、④有关反应的离子方程式:
①产生白色沉淀
②产生气体
④产生白色沉淀
(3)有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)