摘要:思考: 1.核外电子排布的规律是怎样?完成下列原子结构示意图: H O O2- Na Al Al3+ S Cl-
网址:http://m.1010jiajiao.com/timu3_id_191830[举报]
A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大。已知B的最外
电子层是ns2npn+1;C的p亚层上未成对的电子比B少一个,D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A能生成具有刺激性气味的气体。
(1)B核外电子排布式为__________________________。
(2)A与E化合时原子间以_____________键相结合,D与C化合时原子间以_____________键相结合。
(3)写出A、C直接形成的化合物与E的单质反应的离子方程式_______________________。
(4)写出B和D形成的化合物遇水时发生反应的方程式______________________________。
查看习题详情和答案>>
A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大。已知B的最外电子层是ns2npn+1;C的p亚层上未成对的电子比B少一个,D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A能生成具有刺激性气味的气体。
(1)B核外电子排布式为__________________________。
(2)A与E化合时原子间以__________键相结合,D与C化合时原子间以__________键相结合。
(3)写出A、C直接形成的化合物与E的单质反应的离子方程式_______________________。
(4)写出B和D形成的化合物遇水时发生反应的方程式______________________________。
查看习题详情和答案>>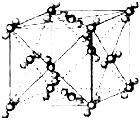 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中B、D、F原子最外电子层的P能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如图所示.E的电负性在该周期中最大.镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaF为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中B、D、F原子最外电子层的P能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如图所示.E的电负性在该周期中最大.镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaF为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.试回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为
(2)A、B、C的第一电离能由大到小的顺序为
(3)B元素的单质分子中有
(4)上述A的氧化物分子中心原子采取
(5)FH3沸点与比BH3
(6)固体CrE3?6H2O溶于水可能有几种不同组成的配离子,实验将含0.2665gCrE3?6H2O的溶液通过H-离子交换树脂(只交换配阳离子),交换出的酸用0.125mol/L的氢氧化钠溶液8.00mL中和.已知配离子配位数为6,则该配离子是
(2009?潍坊一模)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个末成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个末成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1.请回答下列问题.
(1)A单质、B单质、化合物R的熔点大小顺序为下列的
①A单质>B单质>R ②R>A单质>B单质
③B单质>R>A单质 ④A单质>R>B单质
(2)CB3分子的空间构型是
(3)写出D原子的核外电子排布式
(4)D和Fe形成一种黄色晶体FeD2,FeD2晶体中阴、阳离子数之比为
查看习题详情和答案>>
(1)A单质、B单质、化合物R的熔点大小顺序为下列的
②
②
(填序号)①A单质>B单质>R ②R>A单质>B单质
③B单质>R>A单质 ④A单质>R>B单质
(2)CB3分子的空间构型是
三角锥
三角锥
,其固体时的晶体类型为分子晶体
分子晶体
.(3)写出D原子的核外电子排布式
1S22S22P63S23P4
1S22S22P63S23P4
,C的氢化物比D的氢化物在水中溶解度大的多的原因氨分子与水分子间形成氢键并发生反应
氨分子与水分子间形成氢键并发生反应
.(4)D和Fe形成一种黄色晶体FeD2,FeD2晶体中阴、阳离子数之比为
1:1
1:1
,FeD2物质中具有的化学键类型为离子键、非极性键
离子键、非极性键
.(2012?太原一模)X、Y、Z、U、W为原子序数依次增大的前四周期元素,X、Y、Z三种元素的基态原子具有相同的能层和能级,且第一电离能:I1(X)<I1(Z)<I1(Y),其中基态Y原子的2p轨道处于半充满状态,且XZ2与Y2Z互为等电子体.U为周期表前四周期中电负性最小的元素,W的原子序数为26.试回答下列问题:
(1)XZ2的电子式为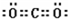
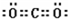 ,基态W原子的核外电子排布式为
,基态W原子的核外电子排布式为
(2)Y的简单氢化物极易溶于Z的简单氢化物中,其主要原因是
(3)X的一种氢化物的相对分子质量为26,其分子中σ键与π键的键数之比为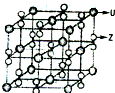
(4)化合物甲由Z、U两元素组成,其晶胞如图所示.
①甲的化学式为
②下列有关该晶体的说法正确的是
A.每个晶胞中含有14个U+和13个Z-2
B.晶体中每个U+周围距离U+最近的Z-2有8个
C.晶体中与每个U+距离最近的U+有12个
D.该晶体属于离子晶体
③甲的密度为a g?cm-3,则晶胞的体积是
cm3(只要求列出计算式,阿伏加德罗常数用NA表示).
查看习题详情和答案>>
(1)XZ2的电子式为
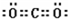
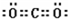
1s22s22p63s23p63d64s2
1s22s22p63s23p63d64s2
.(2)Y的简单氢化物极易溶于Z的简单氢化物中,其主要原因是
这两种氢化物均为极性分子,氨气和水分子之间能形成氢键
这两种氢化物均为极性分子,氨气和水分子之间能形成氢键
.(3)X的一种氢化物的相对分子质量为26,其分子中σ键与π键的键数之比为
3:2
3:2
;其分子中X原子的杂化轨道类型为sp
sp
.
(4)化合物甲由Z、U两元素组成,其晶胞如图所示.
①甲的化学式为
KO2
KO2
②下列有关该晶体的说法正确的是
CD
CD
(填字母编号).A.每个晶胞中含有14个U+和13个Z-2
B.晶体中每个U+周围距离U+最近的Z-2有8个
C.晶体中与每个U+距离最近的U+有12个
D.该晶体属于离子晶体
③甲的密度为a g?cm-3,则晶胞的体积是
| 284 |
| aNA |
| 284 |
| aNA |