摘要: 已知X为ⅠA族元素.Y为ⅥA族元素.则X.Y形成化合物的化学式不可能为 A.X2Y B.X2Y2 C.XY2 D.XY3
网址:http://m.1010jiajiao.com/timu3_id_188945[举报]
已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为气体单质,D为无色气体,在空气中会出现红棕色.各物质的转化关系如图(部分反应产物已略去).

请回答下列问题:
(1)X的化学式为
(2)在反应①②③④中属于置换反应的是
(3)反应②的离子方程式为
(4)X溶液与F反应的总化学方程式为
(5)若向100mL 盐X的溶液中加入10g金属单质M的粉末,充分搅拌后,过滤,烘干得10.16g固体C.则滤液A中溶质的物质的量浓度为
查看习题详情和答案>>

请回答下列问题:
(1)X的化学式为
Cu(NO3)2
Cu(NO3)2
.(2)在反应①②③④中属于置换反应的是
①③
①③
(填序号).(3)反应②的离子方程式为
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
.(4)X溶液与F反应的总化学方程式为
2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2+4NaNO3+O2↑
2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2+4NaNO3+O2↑
.(5)若向100mL 盐X的溶液中加入10g金属单质M的粉末,充分搅拌后,过滤,烘干得10.16g固体C.则滤液A中溶质的物质的量浓度为
0.2mol/L
0.2mol/L
.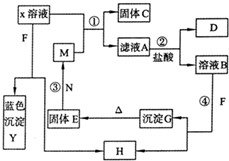 (2009?滨州模拟)已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色.各物质的转化关系如图(部分反应产物已略去).
(2009?滨州模拟)已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色.各物质的转化关系如图(部分反应产物已略去).请回答下列问题;
(1)E的化学式为
Fe2O3
Fe2O3
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是
铁丝上附有红色物质,溶液颜色逐渐变为浅绿色
铁丝上附有红色物质,溶液颜色逐渐变为浅绿色
.(3)在反应①②③④中属于置换反应的是
①③
①③
(填序号)(4)反应②的离子方程式为
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
.(5)用石墨作电极点解500mLX溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;点解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g.请回答下列问题:
①写出点解时的阳极反应式
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
.②电解后溶液的pH为
1
1
(假设电解前后溶液体积不变).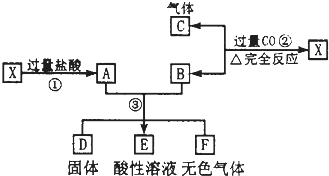 已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):
已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):(1)写出物质D的化学式:
(2)若所得固体D的质量为32g,溶液E中只含一种金属离子,气体F在标准状况下体积为5.6L,试计算X中FeO与CuO的质量比(写出计算过程).
 已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).
已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).请回答下列问题;
(1)E的化学式为
Fe2O3
Fe2O3
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:
铁丝上附有红色物质,溶液颜色逐渐变为浅绿色
铁丝上附有红色物质,溶液颜色逐渐变为浅绿色
.(3)反应①②③④中属于置换反应的是
①③
①③
(填序号).(4)反应②的离子方程式为
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g.
请回答下列问题:
①写出电解时的阳极反应式
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
②电解一段时间后转移
0.05
0.05
mol电子,溶液的pH降低
降低
(填“升高”、“不变”、“降低”) 已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )