题目内容
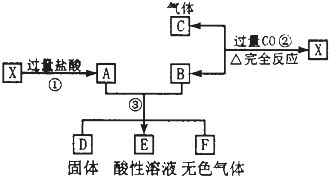 已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):
已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):(1)写出物质D的化学式:
(2)若所得固体D的质量为32g,溶液E中只含一种金属离子,气体F在标准状况下体积为5.6L,试计算X中FeO与CuO的质量比(写出计算过程).
分析:X为FeO和CuO的混合物,由转化关系可知,A中含HCl、FeCl2、CuCl2,B中含Fe、Cu,C为CO2,B与A反应生成F为H2,还原性Fe>Cu,则Fe与A中阳离子反应,固体D为Cu,E为一定含FeCl2,以此来解答.
解答:解:X为FeO和CuO的混合物,由转化关系可知,A中含HCl、FeCl2、CuCl2,B中含Fe、Cu,C为CO2,B与A反应生成F为H2,还原性Fe>Cu,则Fe与A中阳离子反应,固体D为Cu,E为一定含FeCl2,
(1)由上述分析可知,D为Cu,
故答案为:Cu;
(2)所得固体D的质量为32g,溶液E中只含一种金属离子,气体F在标准状况下体积为5.6L,
a.由Fe+2H+═Fe2++H2↑,
可知与盐酸反应的Fe的质量为:
×56g?mol-1=14g,
b.由题意一份X中含Cu的质量为32 g÷2=16 g,
由 Cu2++Fe═Fe2++Cu 差量
64 56 8
16g
得16 g Cu2+与Fe反应的差量为
=2 g,
与16 g Cu2+反应的Fe的质量为
=14 g,
所以一份X中含Fe的质量为14 g+14g=28 g,
c.X中FeO与CuO的质量比为
×72g?mol-1:
×80g?mol-1=9:5,
故答案为:9:5.
(1)由上述分析可知,D为Cu,
故答案为:Cu;
(2)所得固体D的质量为32g,溶液E中只含一种金属离子,气体F在标准状况下体积为5.6L,
a.由Fe+2H+═Fe2++H2↑,
可知与盐酸反应的Fe的质量为:
| 5.6L |
| 22.4L?mol-1 |
b.由题意一份X中含Cu的质量为32 g÷2=16 g,
由 Cu2++Fe═Fe2++Cu 差量
64 56 8
16g
得16 g Cu2+与Fe反应的差量为
| 16g×8 |
| 64 |
与16 g Cu2+反应的Fe的质量为
| 56×2g |
| 8 |
所以一份X中含Fe的质量为14 g+14g=28 g,
c.X中FeO与CuO的质量比为
| 28g |
| 56g?mol-1 |
| 16g |
| 64g?mol-1 |
故答案为:9:5.
点评:本题考查无机物的推断,侧重金属与酸的反应及有关计算的考查,(2)中计算为解答的难点,注意Fe参与的反应分析其质量即可解答,题目难度中等.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
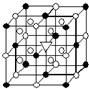 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子