摘要:下图所涉及的物质均为中学化学中的常见物质.其中C为O2.D为C12.E为Fe单质.其余为化合物.它们存在如下转化关系. 反应中生成的水及次要产物均已略去. (1)写出有关物质的名称或化学式: B .F .H . (2)指出MnO2在相关反应中的作用:反应①中是 剂.反应②中是 剂. (3)若反应①是在加热条件下进行.则A是 ,若反应①是在常温条件下进行.则A是 . (4)写出B与MnO2共热获得D的化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_187137[举报]
(2009?长春一模)下图所涉及的物质均为中学化学中常见的物质,其中C、D为气体单质,E为常见金属单质,其余为化合物,F晶体具有磁性,它们之间存在如下转化关系(部分产物已省略).
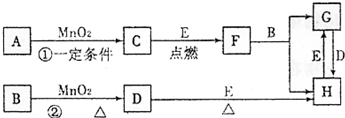
请回答下列问题:
(1)若反应①是在加热条件下进行的,则A是(填化学式)
(2)写出②的离子反应方程式:
(3)H用途广泛,如用作催化剂,印刷电路腐蚀剂和外伤止血济及净水等.若将Cu棒与碳棒用导线连接并插入H溶液中,可形成原电池,其中正极电极反应方程式为:
(4)写出G与D反应生成H的化学方程式为:
查看习题详情和答案>>

请回答下列问题:
(1)若反应①是在加热条件下进行的,则A是(填化学式)
KClO3
KClO3
;若反应①是在常温条件下进行的,则A是(填化学式)H2O2
H2O2
;若在上述两种条件下得到等量的C单质,反应中转移的电子数之比为2:1
2:1
.(2)写出②的离子反应方程式:
MnO2+4H++2Cl-
Cl2+Mn2++2H2O
| ||
MnO2+4H++2Cl-
Cl2+Mn2++2H2O
.
| ||
(3)H用途广泛,如用作催化剂,印刷电路腐蚀剂和外伤止血济及净水等.若将Cu棒与碳棒用导线连接并插入H溶液中,可形成原电池,其中正极电极反应方程式为:
Fe3++e-=Fe2+
Fe3++e-=Fe2+
.(4)写出G与D反应生成H的化学方程式为:
2FeCl2+Cl2=2FeCl3
2FeCl2+Cl2=2FeCl3
.(2008?湖南模拟)下图所涉及的物质均为中学化学中常见的物质,其中C、D、E为单质,其余为化合物,其中纳米F晶体材料可作为核磁共振造影增强剂,可用于疾病的诊断和药物载体,它们之间存在如下转化关系(部分产物已省略).

请回答下列问题:
(1)若反应①是在加热条件下进行的,则A是(填化学式)
(2)H用途广泛如用作催化剂,印刷电路腐蚀剂和外伤止血剂及净水等.若将Cu棒与C棒用导线连接并插入H溶液中,可形成原电池,其中正极电极反应方程式为:
(3)经测定A为二元弱酸,其酸性比碳酸弱,写出A在水溶液中的电离方程式:
A与氨气反应生成的酸式盐的化学式为:
查看习题详情和答案>>

请回答下列问题:
(1)若反应①是在加热条件下进行的,则A是(填化学式)
KClO3
KClO3
;若反应①是在常温条件下进行的,则A是(填化学式)H2O2
H2O2
;若在上述两种条件下得到等量的C单质,反应中转移的电子数之比为2:1
2:1
.(2)H用途广泛如用作催化剂,印刷电路腐蚀剂和外伤止血剂及净水等.若将Cu棒与C棒用导线连接并插入H溶液中,可形成原电池,其中正极电极反应方程式为:
2Fe3++2e-=2Fe2+
2Fe3++2e-=2Fe2+
.总离子方程式为:2Fe3++Cu=2Fe2++Cu2+
2Fe3++Cu=2Fe2++Cu2+
.F与B反应的离子方程式为:Fe304+8H+=2Fe3++Fe2++4H2O
Fe304+8H+=2Fe3++Fe2++4H2O
.(3)经测定A为二元弱酸,其酸性比碳酸弱,写出A在水溶液中的电离方程式:
H2O2=H++HO2-(HO2+=H++O22-)
H2O2=H++HO2-(HO2+=H++O22-)
.A与氨气反应生成的酸式盐的化学式为:
NH4HO2
NH4HO2
.若将适量MnO2加入酸化后的A溶液中,MnO2溶解产生 Mn2+,该反应的离子方程式为:MnO2+H2O2+2H+=Mn2++O2↑+2H2O
MnO2+H2O2+2H+=Mn2++O2↑+2H2O
.(11分)下图所涉及的物质均为中学化学中的常见物质,其中C为气体单质一种主要成分、D在常温下是黄绿色气体、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的化学式
F ,G ,H 。
(2)指出MnO2在相关反应中的作用,反应①中是 剂,反应②中是 剂。
(3)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A的电子式为 。
(4)写出B与MnO2共热获得D的离子方程式
。
(5)写出B与F反应的化学方程式 。
查看习题详情和答案>>
 质,它们存在如下转化关系:
质,它们存在如下转化关系: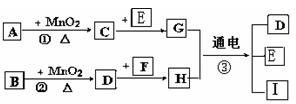
 _______________________
_______________________