摘要:已知NH3气体34 g.求: (1)NH3的物质的量为 . (2)NH3所含原子总数为 . (3)NH3在标准状况下的体积为 . (4)NH3溶于水后形成2L溶液.其溶液的物质的量浓度为 .
网址:http://m.1010jiajiao.com/timu3_id_182987[举报]
已知NH3气体极易溶于水,通常情况下,1体积水里可以溶解700体积NH3。在体积为6 L的干燥烧瓶中,用排空气集气法收集NH3气体后,测得烧瓶内的混合气体对氢气的相对密度为10.5,以此气体进行喷泉实验,当喷泉停止后,进入烧瓶中液体的体积为( )
A.6 L B.5 L C.4 L D.2 L
查看习题详情和答案>>
已知:N2(g)+3H2(g) 2NH3(g);△H=-Q kJ?mol-1(Q>0).现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ.已知Q2=3Q1,下列叙述中正确的是( )
2NH3(g);△H=-Q kJ?mol-1(Q>0).现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ.已知Q2=3Q1,下列叙述中正确的是( )
 2NH3(g);△H=-Q kJ?mol-1(Q>0).现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ.已知Q2=3Q1,下列叙述中正确的是( )
2NH3(g);△H=-Q kJ?mol-1(Q>0).现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ.已知Q2=3Q1,下列叙述中正确的是( )科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和另一种常见气体.进一步研究NH3生成量与温度的关系(其它条件均相同),部分实验数据见下表:
回答下列问题:
(1)写出该反应的化学方程式
(2)请在答题纸的坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注
 .
.
(3)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:
(4)已知:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ/mol
N2(g)+2H2(g)+
Cl2(g)═NH4Cl(s)△H=-313.6kJ/mol
①计算NH3(g)+HCl(g)═NH4Cl(s)的反应焓变:△H=
②室温下NH3就和HCl能发生化合反应生成NH4Cl;而在加热的条件下,NH4Cl则能分解为NH3和HCl.请用所学的化学原理解释这一现象:
查看习题详情和答案>>
| T/K | 303 | 313 | 323 |
| 平衡时NH3的生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
(1)写出该反应的化学方程式
2N2+6H2O
4NH3+3O2
| ||
2N2+6H2O
4NH3+3O2
| ||
(2)请在答题纸的坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注


(3)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:
升高温度,增大反应物N2的浓度
升高温度,增大反应物N2的浓度
.(4)已知:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
①计算NH3(g)+HCl(g)═NH4Cl(s)的反应焓变:△H=
-175.1 kJ/mol
-175.1 kJ/mol
②室温下NH3就和HCl能发生化合反应生成NH4Cl;而在加热的条件下,NH4Cl则能分解为NH3和HCl.请用所学的化学原理解释这一现象:
NH3(g)+HCl(g)═NH4Cl(s)是一个焓减、熵减的反应,在低温下自发,在高温(加热条件)下不自发.而其逆反应NH4Cl的分解则在高温下自发
NH3(g)+HCl(g)═NH4Cl(s)是一个焓减、熵减的反应,在低温下自发,在高温(加热条件)下不自发.而其逆反应NH4Cl的分解则在高温下自发
. 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
③H2O(g)=H2O(l)△H=-44.0kJ?mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为
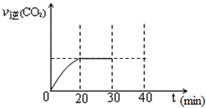
(3)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol?L-1 时间/min |
NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
②根据表中数据,计算T1℃时该反应的平衡常数为
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
④下列各项能作为判断该反应达到平衡的是
A.容器内压强保持不变 B. 2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是
X~W是元素周期表中的短周期元素,其性质或结构信息如下表:
回答下列问题:
(1)X在元素周期表中的位置是
 .
.
(2)Z的单质特别稳定,原因在于
(3)X的氢化物和Z的氢化物反应形成的化合物溶于水,水溶液呈酸性的原因是
(4)WV2常温下呈液态,是一种常见的溶剂.已知WV2在氧气中完全燃烧,生成VO2和WO2,若0.1mol WV2在1mol O2中完全燃烧,所得气体混合物在标准状况下的体积为
(5)已知:①Z2(g)+O2(g)=2ZO(g)△H=+180kJ?mol-1;
②2ZO2(g)=Z2(g)+2O2(g)△H=-67.8kJ?mol-1.
则反应4ZO(g)=2ZO2(g)+Z2(g)的△H为
查看习题详情和答案>>
| 元素 | X | Y | Z | V | W |
| 性质 信息 |
单质为有色气体,有毒,可用于自来水消毒 | 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 | 其单质在空气中约占4/5左右 | 单质为淡黄色晶体,质脆,不溶于水,微溶于酒精 | 位于第IVA,是形成的化合物最多的元素之一 |
(1)X在元素周期表中的位置是
第三周期ⅦA族
第三周期ⅦA族
,V2-离子结构示意图为

(2)Z的单质特别稳定,原因在于
氮气分子中氮氮键为氮氮叁键,键长短,键能大,难断裂
氮气分子中氮氮键为氮氮叁键,键长短,键能大,难断裂
;X、Y和V三元素中原子半径最大的是X(或Cl)
X(或Cl)
.(3)X的氢化物和Z的氢化物反应形成的化合物溶于水,水溶液呈酸性的原因是
NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
(用离子方程式说明).(4)WV2常温下呈液态,是一种常见的溶剂.已知WV2在氧气中完全燃烧,生成VO2和WO2,若0.1mol WV2在1mol O2中完全燃烧,所得气体混合物在标准状况下的体积为
22.4
22.4
L.(5)已知:①Z2(g)+O2(g)=2ZO(g)△H=+180kJ?mol-1;
②2ZO2(g)=Z2(g)+2O2(g)△H=-67.8kJ?mol-1.
则反应4ZO(g)=2ZO2(g)+Z2(g)的△H为
-292.2
-292.2
kJ?mol-1.