摘要: 下图为四种粒子的结构示意图,完成以下填空: A B C D (1)属于原子结构的粒子是 .属于阴离子结构的粒子是 .属于阳离子结构的粒子是 , (2)B粒子的半径 D粒子的半径,(填“大于 .“小于 或“等于 ) (3)某元素X形成的氧化物为X2O.则X的离子结构示意图可能是 .
网址:http://m.1010jiajiao.com/timu3_id_181635[举报]
下图为四种粒子的结构示意图,完成以下填空:

(1)属于阳离子结构的粒子是
(2)B粒子的半径
(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是
查看习题详情和答案>>

(1)属于阳离子结构的粒子是
B
B
.(2)B粒子的半径
小于
小于
C粒子的半径(填“大于”“小于”或“等于”).(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是
D
D
.
下图为四种粒子的结构示意图,完成以下填空:

(1)属于阳离子结构的粒子是______.
(2)B粒子的半径______C粒子的半径(填“大于”“小于”或“等于”).
(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是______.
查看习题详情和答案>>

(1)属于阳离子结构的粒子是______.
(2)B粒子的半径______C粒子的半径(填“大于”“小于”或“等于”).
(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是______.
查看习题详情和答案>>
有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Z2的电子式为 ,Y的原子结构示意图为 ,YW2的结构式为 。
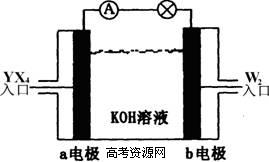
(2)将YX4、W2按上图所示通入某燃料电池中,则两极的电极方程式分别为:
a电极: ,b电极: 。若有16gW2参加反应,转移的电子数是 。
(3)已知在120℃、101kPa下, 0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,该反应的热化学方程式为 。
(4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,则该物质属于 晶体,该晶体中各粒子均满足8电子稳定结构,则化学式为 。
查看习题详情和答案>>(2013?重庆二模)有X、Y、Z、W四种含14个电子的粒子,其结构特点如下:
(1)A原子核外比X原子多3个电子,A的原子结构示意图是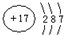
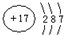
含1mol X的氧化物晶体中含有共价键数目为
(2)Z与钙离子组成的化合物的电子式为

(3)14g Y完全燃烧放出的热量是141.5kJ,写出Y燃烧的热化学方程式
(4)组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系(反应条件和其他物质已略)
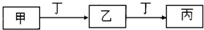
①写出丁在高温下与水反应的化学方程式
②组成W的元素的简单氢化物极易溶于水的主要原因是
查看习题详情和答案>>
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
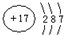
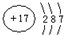
含1mol X的氧化物晶体中含有共价键数目为
4NA
4NA
(2)Z与钙离子组成的化合物的电子式为


(3)14g Y完全燃烧放出的热量是141.5kJ,写出Y燃烧的热化学方程式
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
(4)组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系(反应条件和其他物质已略)

①写出丁在高温下与水反应的化学方程式
3Fe+4H2O(g)
Fe3O4+4H2或C+H2O(g)
CO+H2
| ||
| ||
3Fe+4H2O(g)
Fe3O4+4H2或C+H2O(g)
CO+H2
| ||
| ||
②组成W的元素的简单氢化物极易溶于水的主要原因是
NH3与H2O间能形成氢键
NH3与H2O间能形成氢键
,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
2NH3-6e-+6OH-=N2+6H2O
.前四周期元素X、Y、Z、W核电荷数依次增加,核电荷数之和为56;Y 原子的M层p轨道有3个未成对电子;Z原子的M层p轨道有4个电子;W原子的L层电子数与最外层电子数之比为8:1,其d轨道中的电子数与最外层电子数之比为5:1.
(1)W原子结构示意图为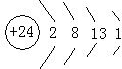
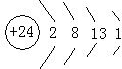 ,W3+的电子排布式为
,W3+的电子排布式为
(2)Y可与X形成只含一个中心原子的共价化合物a,其电子式是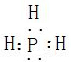
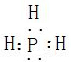 ;中心原子的杂化方式为
;中心原子的杂化方式为
(3)Z最高价氧化物的水化物结构式为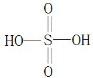
 ,碳元素与Z按1:2的原子个数比形成的b,写出一种与b互为等电子体且含有Z原子的微粒的化学式
,碳元素与Z按1:2的原子个数比形成的b,写出一种与b互为等电子体且含有Z原子的微粒的化学式
(4)Y与Z比较,电负性较大的
查看习题详情和答案>>
(1)W原子结构示意图为
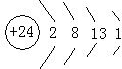
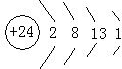
1s22s22p63s23p63d3
1s22s22p63s23p63d3
.(2)Y可与X形成只含一个中心原子的共价化合物a,其电子式是
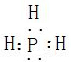
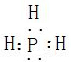
sp3
sp3
;a分子的立体构型是三角锥形
三角锥形
.(3)Z最高价氧化物的水化物结构式为


SCN-或COS
SCN-或COS
.(4)Y与Z比较,电负性较大的
S
S
,1mol单质Y4与3mol氧气在一定条件下完全反应生成1mol化合物c,一个c分子中所含有的σ键数目为12
12
.