摘要:在反应(浓)中. 是氧化剂. 是氧化产物.3mol参加该反应时.反应中转移 mol.
网址:http://m.1010jiajiao.com/timu3_id_180586[举报]
在反应MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O中,
(1)被氧化的元素是
(2)被氧化的HCl与参加反应的HCl的物质的量之比为
(3)请在题中用双线桥法标明电子转移的方向和数目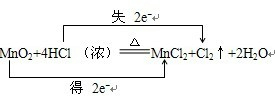
 .
.
查看习题详情和答案>>
| ||
(1)被氧化的元素是
Cl
Cl
,氧化剂是MnO2
MnO2
,氧化产物是Cl2
Cl2
.(2)被氧化的HCl与参加反应的HCl的物质的量之比为
1:2
1:2
(3)请在题中用双线桥法标明电子转移的方向和数目


在反应中:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
(1)
(2)Cu发生了
(3)用双线桥标出反应的电子转移方向和数目:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,若有1.5molCu发生了反应,则转移的电子的个数是
查看习题详情和答案>>
(1)
S
S
元素被还原;H2SO4
H2SO4
是氧化剂(填元素符号或化学式)(2)Cu发生了
氧化
氧化
反应;若某元素的化合价升高了,则该元素所在的生成物称为氧化产物,该反应的还原产物是SO2
SO2
.(填元素符号或化学式)(3)用双线桥标出反应的电子转移方向和数目:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,若有1.5molCu发生了反应,则转移的电子的个数是
3NA
3NA
.在反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中:
(1) 元素得电子, 元素被氧化(填元素名称)。
(2)氧化产物与还原产物的粒子数目之比为_________,氧化剂与还原剂的粒子数目之比是 。
(3)若有7.3gHCl被氧化,则产生Cl2的质量为_______g。
(4)该反应的离子方程式为 。
查看习题详情和答案>>