摘要:5.室验室制取的氯气中混有氧化氢.除去氯化氢气体最好采用的物质是( ) A.水 B.NaOH溶液 C.饱和食盐水 D.氨水
网址:http://m.1010jiajiao.com/timu3_id_180038[举报]
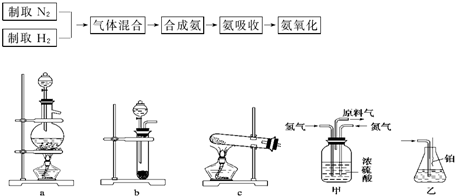
实验室模拟合成氨和氨催化氧化的流程如下:?
已知
A.实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
B.锥形瓶中的铂丝是氨催化氧化反应的催化剂
(1)从上图中选择制取气体的合适装置:氮气
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还可以
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
(5)写出乙装置中氨氧化的化学方程式:
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、
查看习题详情和答案>>

已知
A.实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
B.锥形瓶中的铂丝是氨催化氧化反应的催化剂
(1)从上图中选择制取气体的合适装置:氮气
a
a
、氢气b
b
.(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还可以
干燥气体
干燥气体
、控制氢气和氮气的流速
控制氢气和氮气的流速
.(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,
不会
不会
(“会”或“不会”)发生倒吸,原因是因为混合气体中含有大量难溶于水的氮气、氢气两种气体
因为混合气体中含有大量难溶于水的氮气、氢气两种气体
.(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
表明氨的催化氧化反应是一个放热反应
表明氨的催化氧化反应是一个放热反应
,锥形瓶中还可观察到的现象是:有红棕色气体产生?
有红棕色气体产生?
.(5)写出乙装置中氨氧化的化学方程式:
4NH3+5O2
4NO+6H2O?
| ||
| △ |
4NH3+5O2
4NO+6H2O?
.
| ||
| △ |
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、
NH4+
NH4+
、NO3-
NO3-
离子. 实验室中所用少量氯气是用下列方法制取的,
实验室中所用少量氯气是用下列方法制取的,4HCl(浓)+MnO2
| ||
(1)该反应的离子方程式为
4H++2Cl-+MnO2
Cl2↑+Mn2++2H2O
| ||
4H++2Cl-+MnO2
Cl2↑+Mn2++2H2O
.
| ||
(2)广口瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大),其作用是
除去氯气中混有的HCl气体
除去氯气中混有的HCl气体
.(3)氯气溶入水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中毒死亡,所以氯气直接排入大气中,会污染环境.实验室中可用
浓氢氧化钠(浓碱)
浓氢氧化钠(浓碱)
溶液来吸收有毒的氯气尾气.(4)用浓盐酸80mL,其溶液密度为1.19g/cm3,溶质的质量分数为36.5%,跟MnO2充分反应,产生了5.6L(标准状况)的氯气.则浓盐酸的物质的量浓度为
11.9mol/L
11.9mol/L
;被氧化的HCl的物质的量为0.5mol
0.5mol
.
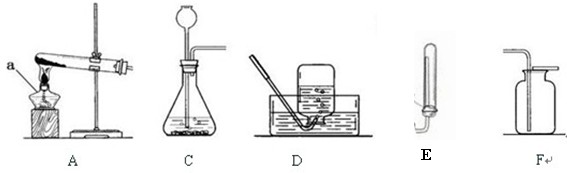
实验室有如图所示的实验装置:

已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.在实验室中通常用加热固体氯化铵和氢氧化钙的混合物来制取氨气.试回答下列问题:
①实验室制取氨气可以选用 装置,收集氨气可以选用 装置.
②试写出实验室制取氨气的化学反应方程式:
③如何检验收集的气体是氨气?试写出方法和结论: .
查看习题详情和答案>>

已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.在实验室中通常用加热固体氯化铵和氢氧化钙的混合物来制取氨气.试回答下列问题:
①实验室制取氨气可以选用
②试写出实验室制取氨气的化学反应方程式:
③如何检验收集的气体是氨气?试写出方法和结论: