摘要:23.将2.0gNaOH溶于水中.要使每100个水分子中溶有1个Na+.则需水的质量为 g.
网址:http://m.1010jiajiao.com/timu3_id_176454[举报]
充分加热碳酸钠和碳酸氢钠的混合物19g,完全反应后固体质量减轻了3.1g,求:
(1)原混合物中碳酸钠的质量.
(2)将原混合物溶于水配成300mL溶液,其中c(Na+)等于多少?
(3)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况).
查看习题详情和答案>>
(1)原混合物中碳酸钠的质量.
(2)将原混合物溶于水配成300mL溶液,其中c(Na+)等于多少?
(3)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况).
有一包白色固体粉末,可能含有Na2SO4,CaCO3,KCl,BaCl2,CuSO4中的一种或几种,按以下步骤进行实验:
(1)将固体粉末溶于水得到无色溶液和白色沉淀;
(2)加以足量的稀盐酸,沉淀部分溶解且有气泡产生.
根据以上实验产生的现象,判断这混合物里,一定含有
写出(1)的反应方程式
写出(2)的反应方程式
查看习题详情和答案>>
(1)将固体粉末溶于水得到无色溶液和白色沉淀;
(2)加以足量的稀盐酸,沉淀部分溶解且有气泡产生.
根据以上实验产生的现象,判断这混合物里,一定含有
Na2SO4,CaCO3,BaCl2
Na2SO4,CaCO3,BaCl2
物质.一定没有CuSO4
CuSO4
物质,可能含有的物质KCl
KCl
.写出(1)的反应方程式
Na2SO4+BaCl2═BaSO4↓+2NaCl
Na2SO4+BaCl2═BaSO4↓+2NaCl
写出(2)的反应方程式
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.Ⅰ.实验室使用容量瓶来配制一定体积、一定浓度的溶液.现在实验室需要0.10mol?L-1NaOH溶液450mL,根据溶液配制中的情况回答下列问题:
(1)实验中除了托盘天平(带砝码)、烧杯、玻璃棒、胶头滴管、药匙外,还需要的仪器有
(2)根据计算得知,需称取NaOH固体的质量为
(3)配制过程中有几个关键的步骤和操作如图1所示,将实验步骤A-F按实验过程先后次序排列
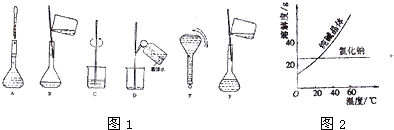
(4)配制一定物质的量浓度溶液的实验中,下列操作会导致溶液浓度偏高的是
A.在托盘天平的两托盘中分别放等质量的纸,称取NaOH固体
B.将NaOH固体在烧杯中溶解后迅速小心转移至容量瓶中
C.定容时不小心加水超过了刻度线,此时迅速用胶头滴管吸出一些
D.定容时仰视容量瓶刻度线
Ⅱ.阅读、分析下列两个材料:
材料一:如图2
材料二:
根据上述材料及课本知识,回答下列问题(填写序号):
A.蒸馏法B.萃取法C.“溶解、结晶、过滤”的方法D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
(2)将乙二醇和丙三醇相互分离的最佳方法是
Ⅲ.有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀.
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体.
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见火焰呈紫色.由上述现象推断:该混合物中一定含有
查看习题详情和答案>>
(1)实验中除了托盘天平(带砝码)、烧杯、玻璃棒、胶头滴管、药匙外,还需要的仪器有
500mL容量瓶
500mL容量瓶
.(2)根据计算得知,需称取NaOH固体的质量为
2.0
2.0
g.(3)配制过程中有几个关键的步骤和操作如图1所示,将实验步骤A-F按实验过程先后次序排列
CBDFAE
CBDFAE
.
(4)配制一定物质的量浓度溶液的实验中,下列操作会导致溶液浓度偏高的是
B
B
.A.在托盘天平的两托盘中分别放等质量的纸,称取NaOH固体
B.将NaOH固体在烧杯中溶解后迅速小心转移至容量瓶中
C.定容时不小心加水超过了刻度线,此时迅速用胶头滴管吸出一些
D.定容时仰视容量瓶刻度线
Ⅱ.阅读、分析下列两个材料:
材料一:如图2
材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 | 乙二醇C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 | 丙三醇C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.蒸馏法B.萃取法C.“溶解、结晶、过滤”的方法D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
C
C
;(2)将乙二醇和丙三醇相互分离的最佳方法是
A
A
.Ⅲ.有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀.
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体.
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见火焰呈紫色.由上述现象推断:该混合物中一定含有
Na2CO3、Na2SO4、Ba(NO3)2
Na2CO3、Na2SO4、Ba(NO3)2
;一定不含有CuCl2、K2CO3
CuCl2、K2CO3
;可能含有NaCl
NaCl
.在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解.试回答下列问题:
(1)FeCl3溶液呈
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是
A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的.
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的.
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的.
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的.
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
查看习题详情和答案>>
(1)FeCl3溶液呈
酸
酸
(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):Fe2++2H2O?Fe(OH)2+2H+
Fe2++2H2O?Fe(OH)2+2H+
;实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,以抑制
抑制
(填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度.(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应
Al3++3HCO3-=Al(OH)3↓+3CO2↑
Al3++3HCO3-=Al(OH)3↓+3CO2↑
.(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是
D
D
.A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的.
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的.
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的.
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的.
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
Al2O3
Al2O3
.(2012?天津模拟)A、B、C、D、E是中学化学常见的5种化合物,其中A、B是氧化物,单质X、Y是生活中常见的金属,试剂1和试剂2分别为常见的酸或碱.相关物质间的转化关系如下图所示(部分反应物与产物已略去):

请回答:
(1)①组成单质X的元素原子结构示意图是
 ;
;
②组成单质Y的元素在周期表中的位置
(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是
(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是
②将物质C溶于水,其溶液呈
(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式
(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.
查看习题详情和答案>>

请回答:
(1)①组成单质X的元素原子结构示意图是


②组成单质Y的元素在周期表中的位置
第四周期第 VIII族
第四周期第 VIII族
.(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是
2Al+2H2O+2OH-=2AlO2-+3H2↑
2Al+2H2O+2OH-=2AlO2-+3H2↑
.(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是
Fe2O3
Fe2O3
.②将物质C溶于水,其溶液呈
酸性
酸性
(填“酸性”、“中性”或“碱性”),原因用离子方程式可表示为Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式
2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
.(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.