题目内容
在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解.试回答下列问题:
(1)FeCl3溶液呈
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是
A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的.
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的.
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的.
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的.
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(1)FeCl3溶液呈
酸
酸
(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):Fe2++2H2O?Fe(OH)2+2H+
Fe2++2H2O?Fe(OH)2+2H+
;实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,以抑制
抑制
(填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度.(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应
Al3++3HCO3-=Al(OH)3↓+3CO2↑
Al3++3HCO3-=Al(OH)3↓+3CO2↑
.(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是
D
D
.A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的.
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的.
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的.
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的.
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
Al2O3
Al2O3
.分析:(1)FeCl3为强酸弱碱盐,溶液呈酸性,溶液中存在Fe2++2H2O?Fe(OH)2+2H+,加入盐酸,抑制水解;
(2)硫酸铝溶液和碳酸氢钠溶液混合时发生Al3+与HCO3-的互促水解反应;
(3)证明盐的水解是吸热的,应改变溶液的温度,根据溶液pH的变化判断;
(4)AlCl3溶液加热促进水解生成Al(OH)3,灼烧时灼烧分解.
(2)硫酸铝溶液和碳酸氢钠溶液混合时发生Al3+与HCO3-的互促水解反应;
(3)证明盐的水解是吸热的,应改变溶液的温度,根据溶液pH的变化判断;
(4)AlCl3溶液加热促进水解生成Al(OH)3,灼烧时灼烧分解.
解答:解:(1)FeCl3为强酸弱碱盐,溶液呈酸性,溶液中存在Fe2++2H2O?Fe(OH)2+2H+,加入盐酸,H+浓度增大,抑制水解,
故答案为:酸;Fe2++2H2O?Fe(OH)2+2H+;抑制;
(2)硫酸铝溶液和碳酸氢钠溶液混合时,由于Al3+水解呈酸性,HCO3-水解呈碱性,则发生Al3+与HCO3-的互促水解反应,方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(3)A.反应为中和反应,放热,不能证明水解,故A错误;
B.硝酸铵晶体溶于水吸热,不能证明水解,故B错误;
C.在氨水加入氯化铵固体,铵根离子浓度增大,平衡向逆反应方向移动,溶液的pH变小,不能说明盐类水解是吸热的,故C错误;
D.在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明升高温度平衡向正反应方向移动,可说明盐类水解是吸热的,故D正确.
故答案为:D;
(4)AlCl3溶液加热促进水解生成Al(OH)3,灼烧时Al(OH)3灼烧分解生成Al2O3,故答案为:Al2O3.
故答案为:酸;Fe2++2H2O?Fe(OH)2+2H+;抑制;
(2)硫酸铝溶液和碳酸氢钠溶液混合时,由于Al3+水解呈酸性,HCO3-水解呈碱性,则发生Al3+与HCO3-的互促水解反应,方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(3)A.反应为中和反应,放热,不能证明水解,故A错误;
B.硝酸铵晶体溶于水吸热,不能证明水解,故B错误;
C.在氨水加入氯化铵固体,铵根离子浓度增大,平衡向逆反应方向移动,溶液的pH变小,不能说明盐类水解是吸热的,故C错误;
D.在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明升高温度平衡向正反应方向移动,可说明盐类水解是吸热的,故D正确.
故答案为:D;
(4)AlCl3溶液加热促进水解生成Al(OH)3,灼烧时Al(OH)3灼烧分解生成Al2O3,故答案为:Al2O3.
点评:本题考查盐类水解的应用,题目难度中等,注意实验设计方案的评价,把握物质的性质是解答该题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列说法错误的是( )
| A、钠在空气中燃烧,所得的产物是Na2O2 | B、铝因在空气中形成了一薄层致密的氧化膜,保护内层金属,表现出良好的抗腐蚀性 | C、二氧化硫能漂白某些物质,说明它具有氧化性 | D、不同价态的铁元素之间的相互转化在生产生活和科学研究中有着很多的应用 |
(12分)在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解。试回答下列问题:
(1)FeCl2溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;实验室在配制FeCl2溶液时,常将FeCl2固体先溶于较浓的盐酸中,以 (填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度。
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应 。
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是 。
| A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的。 |
| B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的。 |
| C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的。 |
| D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的。 |

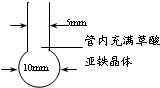 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.